Detección de cerdas púber e impúber por ecografía con sonda W3
Ecografía reproductiva:
Una herramienta diagnóstica del presente y futuro
Desde hace 30 años, a través del desarrollo de tecnología y portabilidad, las técnicas ecográficas en tiempo real (B-Mode) se han convertido en una valiosa herramienta de diagnóstico reproductivo, siendo rápidamente introducidas en la industria porcina como complemento para determinar la confirmación de preñez (Kauffold et al, 2019). La introducción de los equipos de ecografía, han permitido a los veterinarios ir más allá del diagnóstico de gestación temprano, obteniendo una serie de aplicaciones con un gran impacto económico en industria porcina (Inaba et al, 1983).
Entre estas aplicaciones destacan la monitorización de la actividad ovárica, la estimación del momento de ovulación, el estado de maduración del aparato reproductor en futuras reproductoras con el fin de determinar el comienzo de la pubertad, así como la determinación de patologías tanto a nivel individual como de grupo, patologías relacionadas con un empeoramiento de los índices técnico-económicos (Martinat-Botté et al, 2002).
Presentación del caso
El caso clínico corresponde con una revisión de las pautas de manejo reproductivo asociadas al control de celos en futuras reproductoras; asimismo al manejo de inseminación artificial sobre las cerdas destetadas.
Dicha revisión se realizó en noviembre de 2019 en una explotación de producción de lechones con fase I y II situado en la provincia de Zaragoza. La explotación cuenta con un censo de 1100 cerdas reproductoras de genética Danbred.
Desde el punto de vista sanitario la explotación es positiva a virus PRRS por serología en reproductoras, pero con resultados negativos a pool de PCR de lechones en el momento del destete. Negativa para disentería y rinitis atrófica. No se han reportado casos asociados a gripe o leptospirosis en los últimos 24 meses.
En relación con sus resultados zootécnicos:
- Nacidos Totales: 16,64
- Nacidos Vivos: 14,90
- Momias: 0,15
- Nacidos Muertos: 1,74
- Destetados: 12,3
- Destete cerda al año: 29,72 lechones
- IDC: 5,4
- Tasa de partos: 86,9
- Lactación: 27 días
- Porcentaje de cerdas eliminadas por año: 52,6%
- Días perdidos por cerda eliminada: 32,6
A pesar de los aparentes buenos resultados, los nacidos totales de las cerdas jóvenes (15,45) y los nacidos totales (16,64) de dicha explotación son significativamente inferiores a la media de los resultados de la integración a la que pertenece la granja, siendo 16,43 y 17,78 respectivamente.
1º.- Manejo reproductivo en futuras reproductoras
Diagnóstico de cerdas jóvenes púberes e impúberes
De un lote de 38 cerdas de 7 meses de edad, se decide realizar un análisis ecográfico con el fin de determinar el porcentaje de cerdas impúberes a esa edad.
Para esto se utilizó el ecógrafo Kubus W3 de sonda sectorial inalámbrica, trabajando a 3,5Mhz con una profundidad de 14 cm y una ganancia de 87%.
El diagnóstico se basó en la determinación del tamaño del útero y su posición en relación con otras estructuras como la vejiga urinaria o las asas intestinales. En general, se encuentra en posición ventral a la vejiga. Cuando el tamaño del útero es pequeño, ocupa muy poco espacio en la pantalla, de esta manera se considera una hembra impúber.
Imágenes de cerdas impúberes con el ecógrafo W3 de Kubus
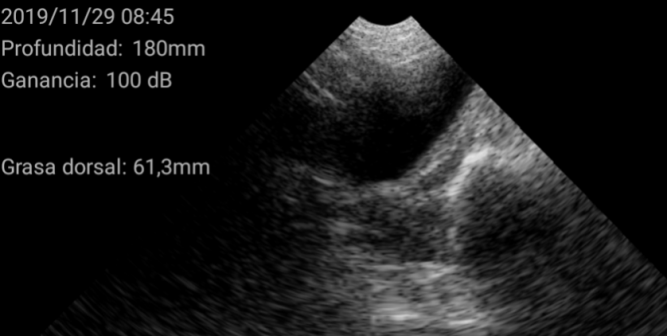
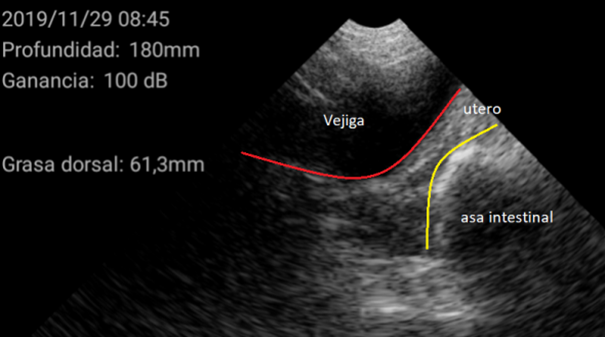
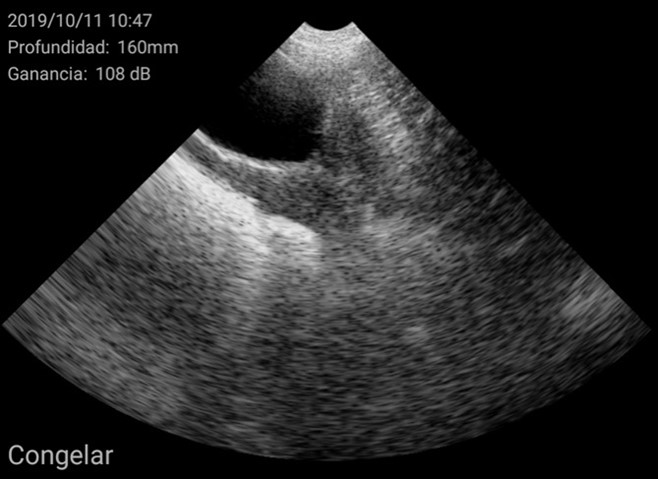
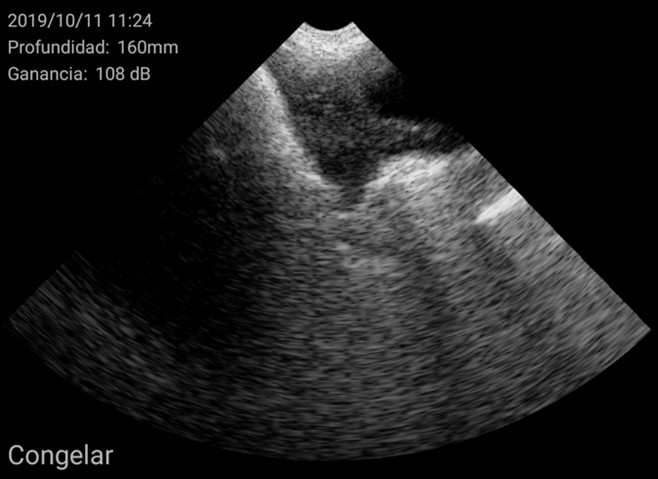
Por el contrario, úteros grandes, con cuernos uterinos identificables y que ocupan gran superficie de la pantalla se consideran como hembra púber.
Imágenes de cerdas Púberes con el ecógrafo W3 de Kubus
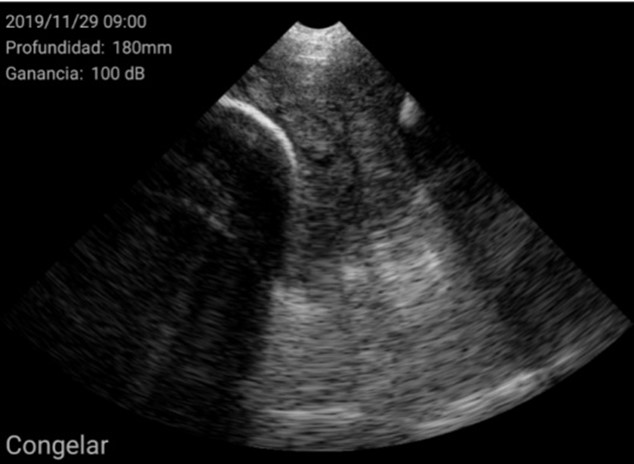
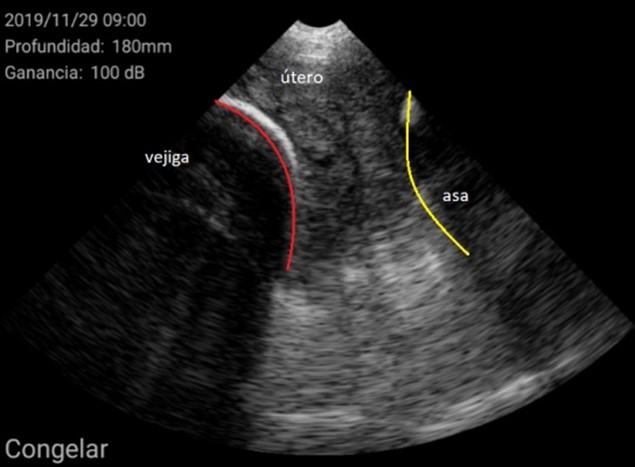
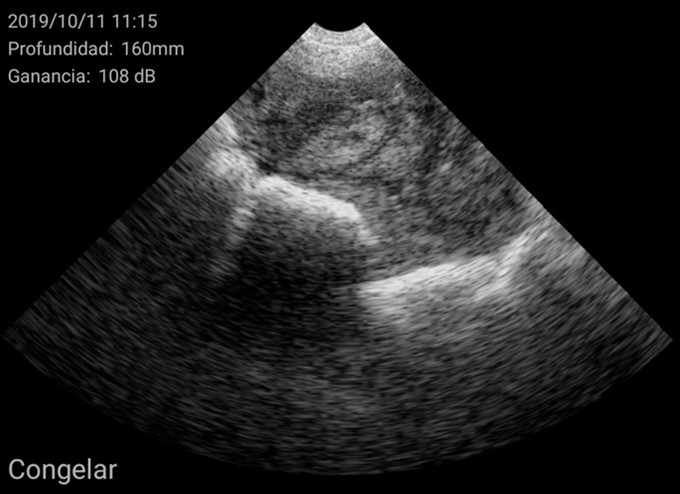
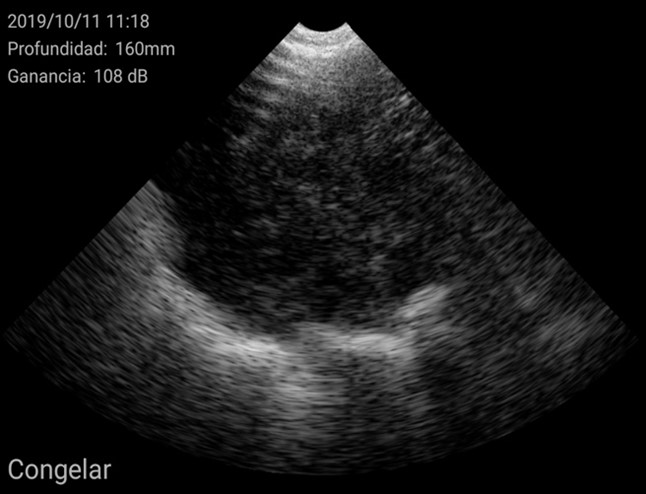
Además, se pudieron identificar otras estructuras como éste ovario con cuerpos hemorrágicos y un folículo central no ovulado, característico de una cerda en metaestro:
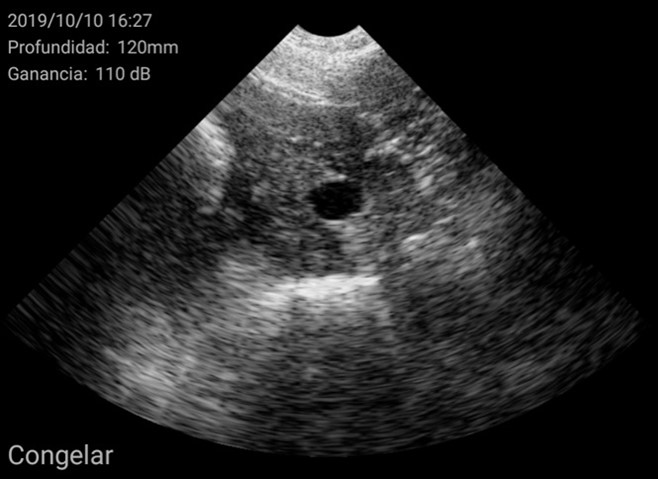
Los resultados indicaron que 12 de las 38 cerdas jóvenes analizadas (31%) resultaron ser impúberes. Un 10-15% mayor de lo esperado. Este alto porcentaje de cerdas impúberes a los 7 meses pueden suponer un mayor porcentaje de cerdas cubiertas en el primer ciclo ya que la edad objetivo de cubrición de la granja es entre los 7,5 y los 8,5 meses de vida.
Está descrito en la bibliografía que la tasa de ovulación del primer celo es significantemente menor que en celos posteriores, lo que podría resultar ser una explicación a sus peores resultados de nacidos totales con respecto a la media de la empresa.
En este caso, se recomendó realizar un seguimiento por ecografía a la semana de entrar en jaula, con un tratamiento con gonadotropinas a todas aquellas cerdas que en ese momento presentaban un diagnóstico de impúberes. La cubrición se realizará en estos casos siempre en el siguiente celo (o posteriores).
2º.- Manejo reproductivo en cerdas destetadas
Dinámica folicular para una inseminación más próxima a la ovulación
Una vez realizadas las ecografías en la zona de preparación de la nulípara, se procedió al diagnóstico ecográfico de las cerdas destetadas en la zona de cubrición, debido a que se reportaba una tasa del 12% de repeticiones en la granja. Para este caso, se realizó un estudio de dinámica folicular. Dicho estudio requiere ser realizado por un profesional en el tema y preferiblemente con equipos de mayor resolución. El procedimiento fue llevado a cabo por Antonio Vela y se empleó un ecógrafo Esaote MyLab Delta, con una sonda microconvexa de 8,5 Mhz.
Los estudios de dinámica folicular permiten predecir el momento de la ovulación en función del tamaño del folículo. Por lo que podemos ajustar el programa de inseminación relacionándolo con el momento de ovulación con respecto al momento de inseminación (Kauffold et al, 2004).
Conociendo la dinámica folicular, se puede predecir el momento de ovulación. Folículos de 3-4mm ovularán en 40 horas, folículos de 5mm ovularán en 32-35 horas, folículos de 6-7 mm ovularán en 24 horas y la ovulación se llevará a cabo cuando el folículo mida entre 8- 9mm (Williams et al, 2017).
Al momento de realizar la ecografía a las hembras recién inseminadas, se observaron folículos de 5 mm y otras que llevaban 24 horas post IA tenían folículos de 5,6mm. En ambos casos se detectó que el personal encargado de las cubriciones, estaban inseminando a las cerdas con muchas horas de anticipo a la ovulación, lo que provoca que la primera dosis seminal se esté desperdiciando, y peor aún, el sistema inmune se active desencadenándose una respuesta inmune e inflamatoria que perjudica el proceso de transporte y capacitación de los espermatozoides, por lo tanto dificulta la fecundación de la segunda dosis. En definitiva, se adecuo el programa de inseminación a su sistema y detección de celo de manera que quedaran las inseminaciones en una horquilla de entre 20 y 4 horas antes de la ovulación. Con esta adecuación, se obtuvo un 94 % de dosis fecundantes vs el 67% inicial.
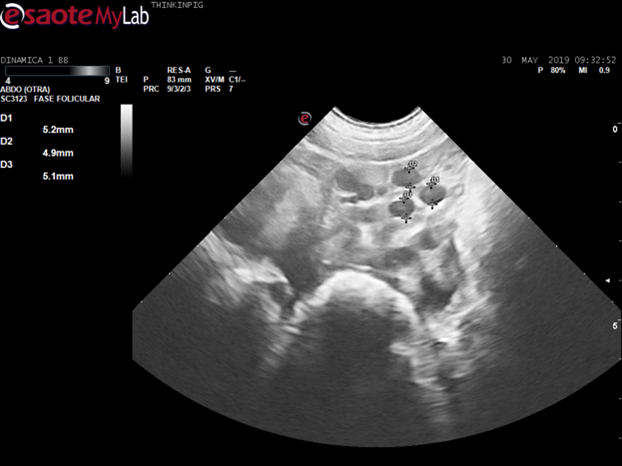
Folículos preovulatorios de 5,2mm (a 37 horas de ovulación). Imagen cedida por A.Vela
Por otra parte, se detectó que aunque la recela se realizaba con un macho adulto y entrenado de una forma correcta, no era suficiente el tiempo en contacto con las hembras para lograr un estímulo en aquellas cerdas que no manifestaban el celo, por lo que se recomendó dejar al verraco más tiempo después de la detección.
Conclusiones:
Desde la década de 1980, contamos con una valiosa herramienta que se ha convertido en un elemento esencial para el diagnóstico y rendimiento reproductivo de la granja.
La combinación de las habilidades de un profesional y un equipo de calidad, nos proporciona un valor añadido para obtener los mejores índices productivos.
No hagamos siempre lo mismo, esperando resultados diferentes. Atrevámonos a utilizar las herramientas que tenemos a la mano como la ecografía y el estudio de la dinámica folicular.
Es fundamental involucrar al personal para que estén motivados a hacer realidad los cambios, ya que serán la clave para ver reflejado el arduo esfuerzo de todo el equipo.
Bibliografía
Inaba, T; Nakazima, Y; Matsui, N; Imori, T; 1983. Early pregnancy diagnosis in sow by ultrasonic linear electronic scanning. Theriogenology 20:97-101.
Kauffold, J,: Peltoniemi, O; Wehrend, A; Althouse, G; Principles and clinical uses of real-time ultrasonography in female swine reproduction. Animals. 9 (2019), doi:10.3390/ani9110950.
Kauffold, J.; Rautenberg, T.; Richter, A.; Waehner, M.; Sobiraj, A. Ultrasonographic characterization of the ovaries and the uterus in prepubertal and pubertal gilts. Theriogenology 2004, 61, 1635–1648.
Martinat-Botté, F., Royer, E., Venturi, E., Boisseau, C., Guillouet, P., Furstoss, V., & Terqui, M. (2003). Determination by echography of uterine changes around puberty in gilts and evaluation of a diagnosis of puberty. Reproduction, nutrition, development, 43 3, 225-36 .
Williams, Sara & de la Sota, Rodolfo Luzbel. (2017). Follicular dynamics and ovulation time in gilts and post-weaning sows. The Canadian veterinary journal. La revue veterinaire canadienne. 58. 65-69.
Reporte elaborado por Marina López.











