Novedades en la prevención de la coccidiosis y la anemia ferrópenica porcinas
Introducción
La coccidiosis provocada por Cystoisospora suis, es una enfermedad que cursa con diarrea y retrasos en el crecimiento en lechones en sus primeros días de vida de todo el mundo. Mundt et al. (2005) describieron en un estudio a gran escala llevado a cabo en 12 países europeos, que la prevalencia total de la enfermedad en granjas era del 69 %. Aunque la mortalidad es baja, la morbilidad suele ser elevada y, dado que la coccidiosis se asocia a menudo con un menor peso en el destete, es probable que se produzcan cuantiosas pérdidas económicas. Tradicionalmente, su prevención se ha basado en la aplicación oral de antiparasitarios frente a los coccidios, tal y como el toltrazurilo.
Por otro lado, la anemia ferropénica porcina también es una de las principales causas responsable de retrasos en el crecimiento en lechones neonatos. La baja cantidad de este micronutriente en la leche materna, junto a la dificultad de los lechones para obtenerlo del ambiente, hace que su prevención pase por inyectar hierro vía intramuscular con la cantidad de hierro adecuada (200 mg) en los primeros días de vida de los animales.
¿Y si minimizamos el estrés ocasionado a los lechones al aplicar estos tratamientos reduciendo el manejo?
Se ha desarrollado recientemente la primera combinación de toltrazurilo y hierro inyectable para el control de la coccidiosis y la prevención de la anemia ferropénica en lechones, Forceris (30 mg toltrazurilo /ml; 133,4 mg/ml de hierro como gleptoferrón). Mediante esta combinación, se reduce el manejo de los animales al eliminar el tratamiento tradicional oral con toltrazurilo, manteniendo el tratamiento inyectable.
¿Existen diferencias entre la disponibilidad del toltrazurilo en el plasma y en los tejidos según la vía de administración (IM vs Oral)?1
Para obtener una respuesta, se desarrolló un estudio experimental cuyo objetivo fue evaluar la disponibilidad del toltrazurilo y su metabolito principal (la toltrazuril sulfona, con gran actividad anticoccidial) en el plasma y en los tejidos en los que se aloja Cystoisospora suis tras la administración oral del producto de referencia e intramuscular (Forceris) de toltrazurilo a lechones.
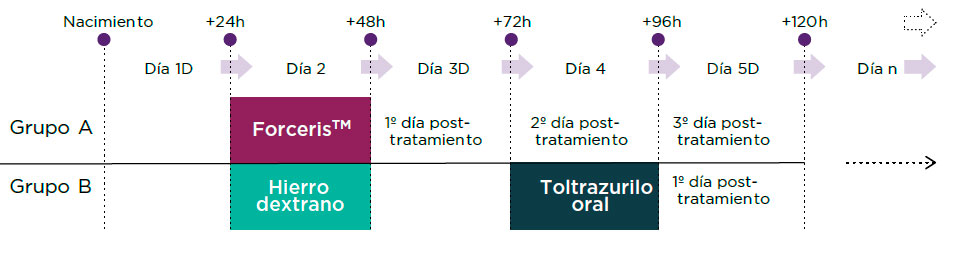
- El grupo A, con 29 lechones, recibió Forceris el segundo día de vida a la dosis recomendada en la ficha técnica (1,5 ml por lechón).
- El grupo B, con 27 lechones, recibió hierro dextrano vía intramuscular el segundo día de vida a la dosis recomendada en la ficha técnica (1 ml por lechón) y toltrazurilo por vía oral el cuarto día de vida (0,4 ml/kg de peso vivo).
Se eutanasiaron un mínimo de 4 lechones a los 1, 5, 13 y 24 días después del tratamiento. De cada lechón se obtuvieron las siguientes muestras: sangre, yeyuno, íleon, contenido del yeyuno y contenido del íleon; y se determinaron las concentraciones de toltrazurilo y su metabolito activo (toltrazuril sulfona) mediante un método validado de HPLC-UV.
En conjunto, la vía intramuscular aportó una concentración significativamente superior y más prolongada en el plasma, los tejidos intestinales (yeyuno, íleon) y el contenido intestinal. Tras la administración vía oral, la concentración en los tejidos solo fue superior en las muestras obtenidas justo después del tratamiento (día 1). Independientemente de la vía de administración, tanto el toltrazurilo como la toltrazurilo sulfona, se acumularon en mayor medida en el segmento proximal del intestino (yeyuno).
Las concentraciones de toltrazurilo (TZ) y toltrazurilo sulfona (TZ-502) tras la administración oral e intramuscular se muestran en las figuras 2 a 5.
C. suis es un parásito intracelular que penetra en los enterocitos del yeyuno y el íleon. La concentración del fármaco en dichos lugares tras su aplicación por vía intramuscular, supone una gran ventaja para sus efectos farmacológicos. Las concentraciones tras la administración i.m. fueron más elevadas y prolongadas, lo que puede explicar su mayor actividad anticoccidial y la reducción significativa de la excreción de ooquistes.
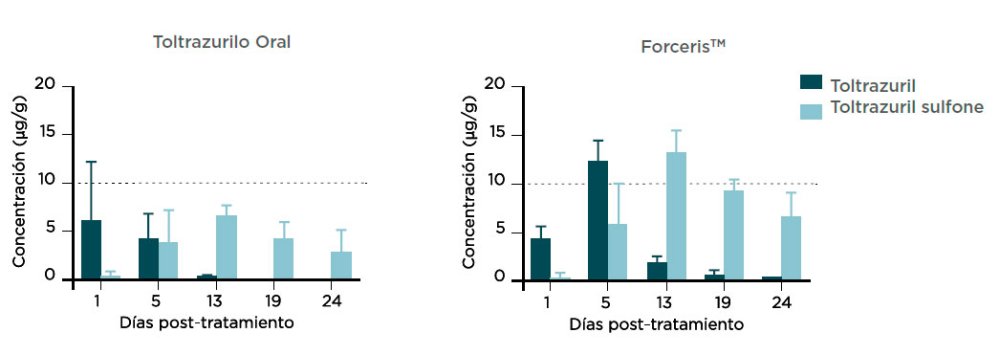
de una sola dosis de ForcerisTM o Baycox 5% a lechones
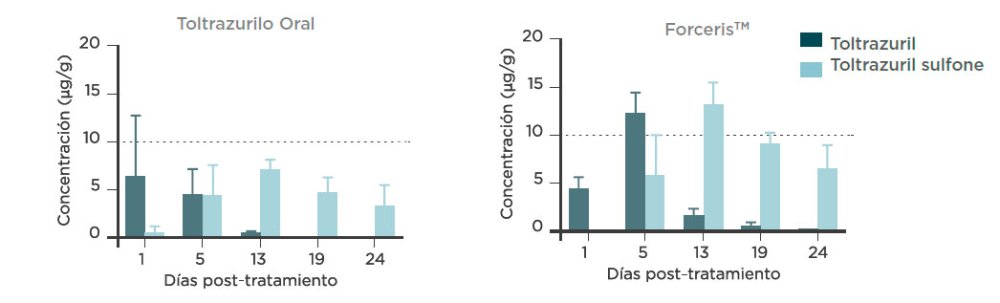
adminsitración de una sola dosis de ForcerisTM o Baycox 5% a lechones
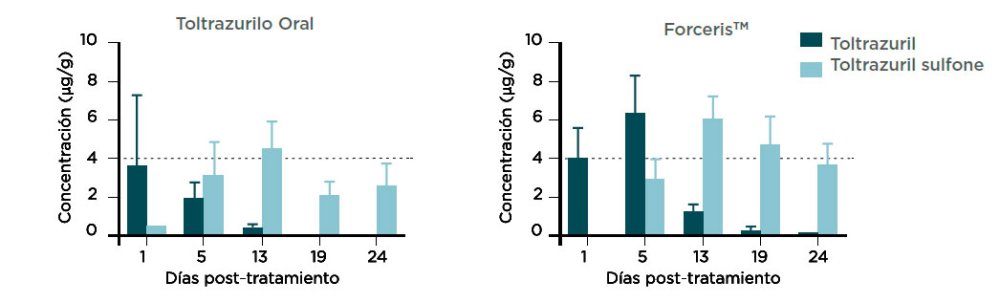
tras la adminsitración a de una sola dosis de ForcerisTM o Baycox 5% a lechones.
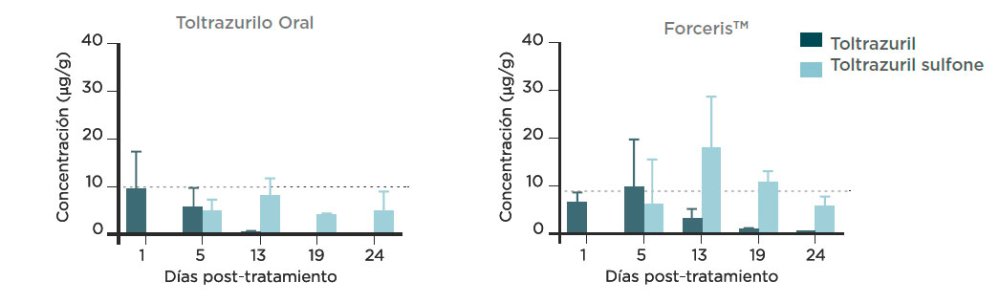
intestinal (mezcla) tras la adminsitración a de una sola dosis de ForcerisTM o Baycox 5% a lechones.
¿Forcersis es eficaz y seguro frente a C. suis en condiciones de campo en granjas con coccidiosis confirmada?2
En este estudio se incluyeron 1.138 lechones, expuestos de forma natural a la coccidiosis, pertenecientes a 4 granjas localizadas en Francia, Alemania y España. Se dividieron a los lechones en:
- Grupo Forceris: 45 mg de toltrazurilo + 200mg de hierro i.m. por lechón el día 1, 2 o 3 de vida
- Grupo Control (CP): 200 mg de hierro i.m. por lechón el día 1 de vida.
Se examinaron las heces según el método de McMaster modificado y se puntuaron de la siguiente forma: 1= sólidas; 2= pastosas; 3= semilíquidas; 4= líquidas. Se consideró diarrea cuando las heces obtenían una puntuación > 2.
Se evaluaron la seguridad (en base a las reacciones locales en el punto de inoculación y la mortalidad), el peso vivo, la excreción de ooquistes y la diarrea.
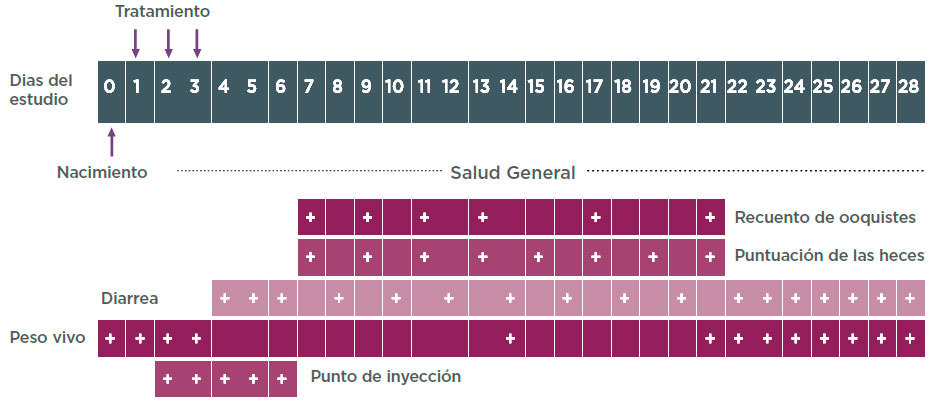
Seguridad:
3 de los 761 lechones (0,4 %) del grupo Forceris mostraron una reacción local transitoria en el punto de inyección.
La mortalidad total predestete fue del 9,1%. En el grupo Forceris, murió un número significativamente menor de lechones (p=0,046) (7,6 %) en comparación con el grupo control (10,6 %).
Peso vivo:
La ganancia media diaria de peso fue significativamente mayor en el grupo Forceris durante el periodo del estudio comprendido entre el día 0 y 14 (p=0,034) y el día 0 y 21 (p=0,004) en comparación con el grupo control (5.936,9 ± 1.821,1 g frente a 5.625,6 ± 1.660,3 g).
Excreción de ooquistes:
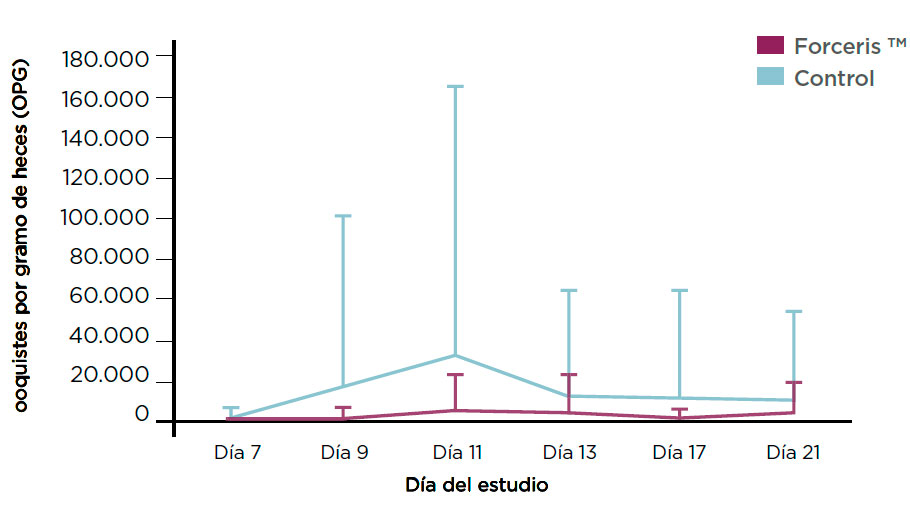
El recuento de ooquistes fue sistemáticamente mayor en el grupo control, que presentó el día 11 un valor medio máximo de 30.403,7 ooquistes por g de heces (OPG). En el grupo Forceris se alcanzó el máximo de la excreción media de ooquistes dos días después, el día 13, y el valor fue claramente menor: 2.506,2 OPG.
El área bajo la curva de la excreción de ooquistes fue significativamente menor en el grupo Forceris en comparación con el grupo control (p < 0,001). El número de muestras fecales con un recuento de ooquistes positivo se redujo en los lechones tratados con Forceris (0,6 muestras, como media) en comparación con el grupo control (1,7 muestras, como media).
Diarrea:
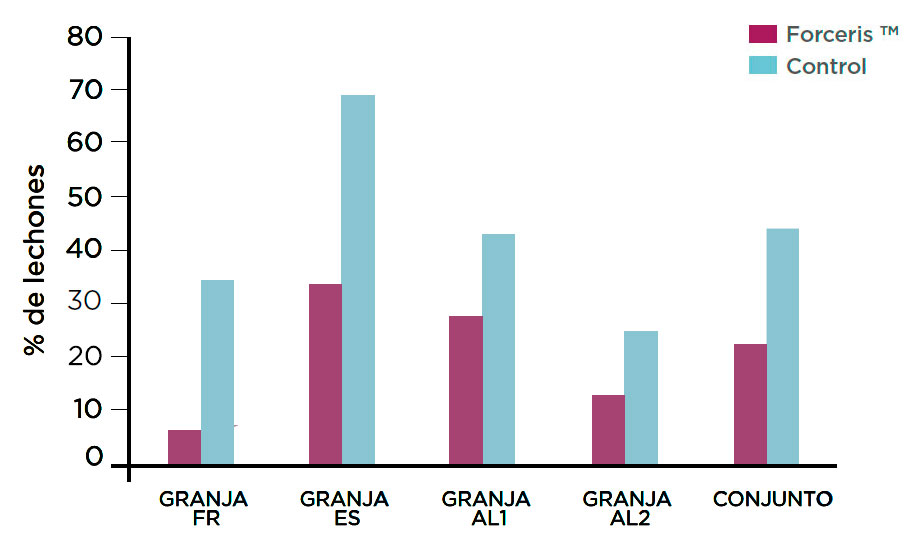
La eficacia de Forceris para controlar la diarrea quedó claramente demostrada en todas las granjas (22,7 % de los lechones con un episodio de diarrea, como mínimo, en el grupo Forceris en comparación con el 44,4 % de los lechones en el grupo control, p <0,001).
Los resultados de este estudio multicéntrico, aleatorizado y enmascarado en lechones infectados de forma natural por C. suis demuestran claramente la eficacia de Forceris con una dosis de 1,5 ml/lechón (45 mg de toltrazurilo y 200 mg de hierro) administrada una sola vez el día 1, 2 o 3 de vida.
Se logró controlar eficazmente la coccidiosis causada por C. suis y los lechones tratados con Forceris mostraron una reducción significativa de la excreción de ooquistes, una menor incidencia de diarrea y una mayor ganancia de peso.
 Conclusiones
Conclusiones
La combinación inyectable de toltrazurilo y hierro administrada poco después del nacimiento es una opción eficaz para controlar la coccidiosis y proporcionar, al mismo tiempo, el suplemento de hierro. De esta manera, disminuye tanto la carga de trabajo como el estrés de los lechones asociado con la manipulación repetida de los animales en granjas con antecedentes confirmados de coccidiosis.
Referencias:
1. Karembe H. et al, 2019, ESPHM Utrech. Plasma disposition kinetics and distribution of toltrazuril and its main metabolite in intestinal tissues and contents of piglets after oral and intramuscular administrations
2. Hiob L. et al, 2019, ESPHM Utrech. Efficacy of an injectable toltrazuril – gleptoferron (Forceris®) to control coccidiosis (Cystoisospora suis) in comparison with iron supplemented piglets without anticoccidial treatment

ForcerisTM 30 mg /ml + 133 mg /ml. Suspensión inyectable para lechones. Composición: cada ml contiene: sustancias activas: toltrazurilo 30,0 mg, hierro (III) 133,4 mg, (como gleptoferron 355,2 mg). Excipientes: fenol 6,4 mg. Especies de destino: porcino (lechones 24 a 96 horas después del nacimiento). Indicaciones de uso: para la prevención simultánea de la anemia por deficiencia de hierro y la prevención de los signos clínicos de la coccidiosis (diarrea) así como la reducción de la excreción de ooquistes en lechones en granjas con antecedentes confirmados de coccidiosis causada por Cystoisospora suis. Contraindicaciones: no usar en lechones de los que se sospecha sufren una deficiencia de vitamina e y/o selenio. Advertencias especiales: como con otros parasiticidas, el uso frecuente y repetido de antiprotozoarios de la misma clase puede conllevar el desarrollo de resistencias. Se recomienda administrar a todos los lechones de cada camada. Una vez que los signos clínicos de coccidiosis sean evidentes, ya se habrá producido un daño en el intestino delgado. Por lo tanto, el producto debe administrarse a todos los animales antes del inicio esperado de los signos clínicos, es decir, en el período de prepatencia. Las medidas higiénicas pueden reducir el riesgo de coccidiosis porcina. Por ello, se recomienda mejorar simultáneamente las condiciones higiénicas en las instalaciones, especialmente la sequedad y la limpieza. El medicamento está recomendado en lechones que pesen entre 0,9 y 3 kg. Precauciones especiales: no debe excederse la dosis recomendada, dado el relativamente bajo margen de seguridad para el medicamento veterinario. El medicamento no debe administrarse más de una vez. No se recomienda usar el medicamento veterinario en lechones que pesen menos de 0,9 kg. Únicamente use este medicamento veterinario en granjas con antecedentes de Cystoisospora suis confirmados. El veterinario responsable debe tener en cuenta los resultados de los exámenes clínicos y/o analíticos de muestras fecales y/o en los hallazgos histológicos que confirmaron la presencia de C. suis en episodios anteriores de infección en la granja. Las personas con hipersensibilidad conocida al hierro (como complejo gleptoferrón), al toltrazurilo o a cualquiera de los excipientes deben evitar todo contacto con el medicamento veterinario. La exposición al medicamento veterinario puede causar irritación en ojos o efectos adversos en la piel. Evite el contacto de la piel y los ojos con el producto. En caso de exposición accidental en piel u ojos, lave el área afectada con agua. La autoinyección accidental puede causar reacciones locales como irritación, granulomas o reacciones anafilácticas graves en personas sensibles. Se debe tener cuidado para evitar la autoinyección accidental. En caso de autoinyección accidental, consulte con un médico inmediatamente y muéstrele el prospecto o la etiqueta. Este medicamento puede ser perjudicial para el feto. Las mujeres embarazadas o que tengan intención de concebir, deben evitar el contacto con el medicamento veterinario, especialmente la autoinyección accidental. Lávese las manos después del uso. Reacciones adversas: se han observado muertes en lechones tras la administración parenteral de inyecciones de hierro en muy raras ocasiones. Estas muertes se han relacionado con factores genéticos o deficiencias en vitamina e y/o selenio. Se han notificado muertes de lechones que se han atribuido a una mayor susceptibilidad a la infección debido al bloqueo temporal del sistema reticuloendotelial. Pueden producirse reacciones de hipersensibilidad. Posología y vía de administración: vía intramuscular. Agitar bien (durante 20 segundos) antes de usar. La dosis recomendada es de 45 mg de toltrazurilo y 200 mg de hierro por lechón, equivalentes a 1,5 ml de Forceris™ por lechón, que se administrará una vez, en una única inyección intramuscular detrás de la oreja, entre 24 y 96 horas después del nacimiento). Tiempos de espera: carne: 70 días. Incompatibilidades principales: en ausencia de estudios de compatibilidad, este medicamento veterinario no debe mezclarse con otros medicamentos veterinarios. Período de validez: período de validez del medicamento veterinario acondicionado para su venta: 3 años. Período de validez después de abierto el envase primario: 28 días. Precauciones especiales de conservación: este medicamento veterinario no requiere condiciones especiales de conservación. Formatos: caja con 1 vial de 250 ml. Precauciones especiales para la eliminación del medicamento veterinario no utilizado o, en su caso, los residuos derivados de su uso: todo medicamento veterinario no utilizado o los residuos derivados del mismo deberán eliminarse de conformidad con las normativas locales. Titular de la autorización de comercialización: Ceva Santé Animale, 10 Av. De la Ballastière, 33500 Libourne, Francia. Número de la autorización de comercialización: eu/2/19/235/001–003.

Ceva Salud Animal - Avenida Diagonal, 609-615, 9ª planta - 08028 Barcelona - Tel: +34 902 367 218 - www.ceva.es
Contacto:
Contacta con nosotros a través del siguiente formulario.