 |
| Cerdos afectados por el PMWS |
En la actualidad, las enfermedades más importantes que afectan a las industrias porcinas a nivel mundial son las enfermedades asociadas con el PCV2 (Circovirus porcino tipo 2) y el PRRS (Síndrome Reproductivo y Respiratorio Porcino). Ambas están íntimamente relacionadas con el Complejo Respiratorio Porcino (CRP) que es, probablemente, el Síndrome más importante de los que afectan a los cerdos, de modo que más del 70% de los diagnósticos de laboratorio corresponden todavía bien a trastornos alimentarios o respiratorios.
Síntomatología
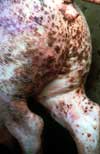 |
| Región perineal de un cerdo con PDNS (agudo, forma hemorrágica similar a la PPC) |
A nivel clínico, los animales pueden dar muestras de enfermedades respiratorias (disnea o tos), pueden tener desmedro o lesiones cutáneas evidentes, o presentar muerte súbita o fracaso reproductivo en su sentido más amplio. Hace varios años, estudiamos las causas potenciales del desmedro en cerdos y descubrimos que había al menos 25 factores posibles que podrían estar implicados: virales, bacterianos, ambientales, del desarrollo y de manejo. Ninguno de estos hallazgos es específico de PCV2 y este agente es sólo uno más de los que podrían estar involucrados.

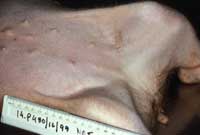 |
| Cerdo en posición dorsal con agrandamiento de los nódulos linfáticos inguinales |
El diagnóstico clínico puede ser más evidente si hay un agrandamiento de los ganglios linfáticos inguinales superficiales por palpación con el cerdo tumbado sobre el dorso y, en ocasiones pueden ser palpables los ganglios superficiales de la cabeza, e incluso los ganglios cervicales superficiales. En casos de PMWS (Síndrome de Desmedro ó Post-weaning Multisystemic Wasting Syndrom), PDNS (Síndrome de Dermatitis y Nefropatía Porcina), Complejo Respiratorio Porcino, Neumonía Proliferativa y Necrotizante Porcina (PNP), posiblemente miocarditis y por supuesto fracaso reproductivo, la inclusión de PCV en la causalidad de los síntomas clínicos sólo se puede demostrar mediante la presencia del agente. Sólo se ha confirmado un papel del PCV2 en los cuatro primeros de estos síndromes.
Diagnóstico laboratorial
Nunca se ha descrito un caso de PMWS de acuerdo con la definición de caso que no haya tenido evidencia de la presencia de PCV2. Esta es por supuesto la obviedad exacta ante la observación de que la mayoría de los cerdos tienen PCV2, pero sólo un porcentaje variable resulta afectado por PMWS y un porcentaje progresivamente menor por PDNS, miocarditis o fracaso reproductivo.
Por lo tanto, la serología es de poca utilidad en la epidemiología de las infecciones por PCV2, ya que el organismo es ubicuo y la mayoría de los cerdos tienen anticuerpos ya sean maternos o adquiridos en el transcurso de una infección neonatal.
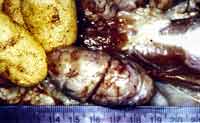 |
| Nódulos linfáticos agrandados |
El diagnóstico de laboratorio para PMWS requiere tejidos linfoides, en particular inguinales, ganglios linfáticos mesentéricos o ileo-ceco-cólicos y traqueo-bronquiales para un examen histopatológico. También el pulmón (tejido linfoide asociado a los bronquios, BALT) y el intestino delgado (placas de Peyer, tejidos linfoides asociados al intestino, GALT) son tejidos muy buenos para evaluar la evidencia histopatológica de PMWS. Las alteraciones histológicas incluyen depleción de linfocitos, inflamación granulomatosa y algunos casos de inclusiones intracitoplásmicas en macrófagos o la presencia de células gigantes multinucleadas. Un estudio reciente en el que estudiamos varios cientos de este grupo de ganglios linfáticos de cerdos, supuestamente infectados con PCV2 (había casos clínicos de granjas con infección conocida) demostró que no había un patrón sistemático en la aparición de ninguna de estas dos características, ni por patología ni por inmunohistoquímica.
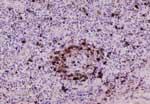 |
| Centro germinal de un cerdo aectado por el PMWS positivo para PCV2 mediante inmunohistoquímica |
La segunda contribución valiosa al diagnóstico de las infecciones por PCV2 exige la demostración del antígeno o el ácido nucleico en los tejidos por hibridación in- situ (HIS) o por inmunohistoquímica (IHQ) o por aislamiento directo del virus a partir de los tejidos. En muchos sentidos, el uso de IHQ es lo mejor, ya que permite relacionar estrechamente la patología revelada por microscopia óptica con la detección del antígeno.
En los casos de PDNS puede haber o no presencia de PCV2. En estos animales que resulten afectados posteriormente de PDNS puede ser que el agente haya desaparecido, lo cierto es que el resultado positivo para PCV2 por IHQ es menor, pero sabemos que la patología es una reacción de hipersensibilidad de tipo 2 y que en el Reino Unido algunas cepas electroforéticas de P. multocida son responsables al menos de las formas esporádicas de PDNS.
El fracaso reproductivo puede estar asociado con infecciones por PCV2, y se puede demostrar la presencia del agente en el feto. Por supuesto, la infección intrauterina del feto producirá miocarditis (un tejido en crecimiento activo en el feto en la fase tardía).
La distinción entre la neumonía intersticial inducida por PCV2 y la observada en CRP solo es posible con IHQ e histopatología, y hasta ahora no se ha podido determinar exactamente cuál es la contribución del PCV2 al CRP.
De igual modo, el diagnóstico histológico de la Neumonía Proliferativa Necrotizante (PNP) puede estar asociado con un diagnóstico etiológico, o bien de PRRS, o Influenza, o PCV2, o posiblemente cualquier combinación, siendo de nuevo la histopatología y la IHQ secuencial las que aportarán la mejor información.
El temblor congénito original de tipo AII descrito por Jack Done se asoció con una pequeña partícula de virus y es sin duda el PCV2 el que tiene el tamaño equivalente, pero hasta ahora, sólo Greg Stevenson en Purdue ha sido capaz de demostrar un resultado positivo para el ácido nucleico de PCV2 en el tejido nervioso y en el hígado de cerdos con temblor congénito y los no afectados. Los últimos estudios realizados en otros centros no han podido reproducir estos descubrimientos hasta ahora.



