El circovirus porcino tipo 2 (PCV2) es conocido como el agente infeccioso principal del llamado síndrome multisistémico de adelgazamiento post-destete (en inglés, postweaning multisystemic wasting syndrome, PMWS), enfermedad también denominada circovirosis porcina (CP). De todas maneras, la CP es un proceso multifactorial donde la participación de este virus parece absolutamente necesaria pero no es suficiente en la mayoría de casos.
Aún existen muchas cuestiones no resueltas sobre la patogenia de esta enfermedad, pero otros aspectos, tal como el diagnóstico, parecen relativamente claros en la actualidad. De hecho, se considera internacionalmente que el diagnóstico de la CP se basa en el cumplimiento de tres criterios:
1) Existencia de un cuadro clínico compatible con la enfermedad (mayoritariamente retraso en el crecimiento, alteraciones respiratorias y mortalidad incrementada).
2) Existencia de lesiones microscópicas caracterizadas por depleción linfocitaria e infiltración granulomatosa de intensidad moderada a marcada en órganos linfoides.
3) Presencia moderada a elevada de PCV2 en los tejidos linfoides lesionados.
Lógicamente, y en base al tercer criterio, se han desarrollado múltiples técnicas para la detección de PCV2. Entre ellas cabe destacar procedimientos sobre tejidos (inmunofluorescencia, inmunohistoquímica, hibridación in situ, PCR estándar y PCR cuantitativa) o sobre suero o excreciones/secreciones corporales (aislamiento vírico, PCR estándar y PCR cuantitativa). De entre todas estas técnicas, la más ampliamente utilizada en distintos laboratorios tanto españoles como a nivel mundial es probablemente la PCR estándar, que permite emitir un resultado positivo (presencia de genoma de PCV2) o negativo (ausencia del mismo).
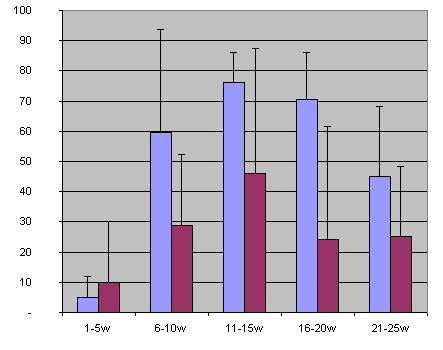

Fig. 1: Medias del porcentaje de cerdos de distintas edades (w = semanas de vida) positivos a PCV2 por PCR en suero. La barra azul representa la media de 4 granjas con CP y la granate de 5 granjas sin CP. Aunque en las granjas con CP hay generalmente un mayor porcentaje de cerdos infectados por PCV2 que las que no tienen la enfermedad, ello no se corresponde en ningún caso con el número de animales enfermos. Gráfica extraída de Sibila y col. (Am J Vet Res, 65:88-92, 2004). Los valores serológicos (datos no mostrados) indican que el 100% de los animales en ambos tipos de granja se acaban infectando a lo largo de su vida productiva.
En la actualidad existen múltiples estudios de comparación de las distintas técnicas de detección de PCV2 y su correlación con enfermedad clínica y presencia de lesiones en órganos linfoides. La mayor parte de estos estudios indican de forma inequívoca que el uso de la PCR estándar para el diagnóstico de la CP es muy poco útil. Ello es debido a que esta técnica no permite discriminar entre infección subclínica por PCV2 (evento que se da en la inmensa mayoría de cerdos en algún momento de su vida productiva, se encuentren sanos o enfermos por otras causas no relacionadas con PCV2) y CP (Fig. 1). Por tanto, un resultado positivo a PCR en ausencia de otras pruebas diagnósticas en un cerdo con retraso en el crecimiento puede corresponder, efectivamente, a un cerdo con CP, pero también a un cerdo cuyo desmedro tenga otra causa distinta a esta enfermedad y que se encuentre concomitantemente infectado por PCV2. Esta situación indica que la PCR no es una técnica fiable para el diagnóstico de la CP. No obstante, cabe destacar que la combinación de la PCR estándar con otros procedimientos laboratoriales, tal como la histopatología principalmente, puede garantizar en mayor medida un diagnóstico más probable de CP.
 |
 |
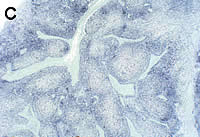 |
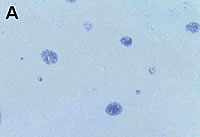
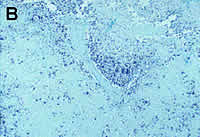
Fig. 2: Hibridación in situ para la detección de PCV2. Se trata de una técnica semicuantitativa que permite correlacionar la cantidad de genoma vírico con las lesiones microscópicas en órganos linfoides. La foto A, la cuál muestra una baja cantidad de genoma vírico, correspondería a una infección subclínica por PCV2 (aunque no podría descartarse una fase pre-clínica de CP o una fase de convalecencia de la enfermedad), mientras que las fotos B y C, con cantidades moderadas a elevadas de virus, corresponderían a cerdos con CP. En todos los casos, la PCR estándar de PCV2 generaría el mismo resultado (positivo), ya que no es una técnica discriminatoria.
La poca utilidad diagnóstica de la PCR estándar para la CP se debe a que esta es una enfermedad en la cuál la cuantificación de PCV2 es crucial. Por tanto, aquellas técnicas que permiten medir cuantitativa o semicuantitativamente el virus, tales como podrían ser la inmunohistoquímica, hibridación in situ (Fig. 2) o PCR cuantitativa (Fig. 3), son las que pueden aportar la seguridad diagnóstica deseada. Quizás el mayor problema de esta demanda es que éstas últimas técnicas no se encuentran ampliamente distribuidas en los Laboratorios de Diagnóstico Veterinario en España; sería de esperar que la implementación de estos procedimientos incrementara ostensiblemente en los próximos años.
Finalmente, y en respuesta a la pregunta planteada en el título, decir que la PCR es una buena herramienta para detectar infección por PCV2 (y por tanto interesante para estudios de dinámica de infección a través de PCR-perfiles), pero una mala herramienta para el diagnóstico de la CP.
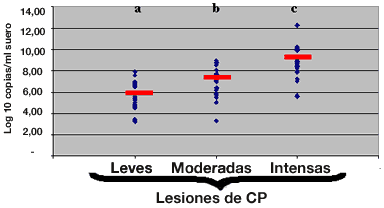
Fig. 3: Cuantificación del genoma de PCV2 en el suero de animales con lesiones microscópicas leves, moderadas e intensas de CP. Las primeras de ellas se corresponderían con cerdos infectados subclínicamente con PCV2. Los valores a, b y c corresponderían a distintos niveles de significancia estadística entre las medias de los distintos grupos lesionales. A tenor de estos resultados se ha propuesto un umbral de 107 genomas de PCV2/ml suero para discriminar entre grupos de animales con y sin CP. Gráfica extraída de Olvera y col. (J Virol Methods, 117:75-80, 2004). En las tres situaciones lesionales, la PCR estándar de PCV2 generaría el mismo resultado (positivo), ya que no es una técnica discriminatoria.



