Introducción a la microbiota intestinal
El tracto gastrointestinal (TGI) del cerdo es el hogar de una población diversa y abundante de bacterias, arqueas, hongos y virus conocidos colectivamente como microbiota. La mayoría de los miembros de esta población se describen como simbióticos, ya que benefician al hospedador de diversas formas, como aumentar la energía que se extrae de la dieta, detoxificar xenobióticos, provisión de nutrientes esenciales, exclusión de patógenos y programación del sistema inmune. Sin embargo, hasta hace poco, la industria porcina se ha centrado en el pequeño porcentaje de la microbiota que representan los patógenos. Es hora de que empecemos a ver la microbiota como fuente de resistencia a enfermedades más que como causa de las mismas.

Desarrollo inmune y resistencia a enfermedades
Para el desarrollo y el funcionamiento adecuados del sistema inmune, es vital que el TGI se colonize tras el nacimiento con microorganismos ambientales. Una microbiota saludable no solo compite con los patógenos por los nutrientes y el espacio, sino que regula la función inmunitaria del hospedador ayudándolo a protegerse a sí mismo tanto de infecciones bacterianas como víricas. Los animales libres de gérmenes tienen un sistema inmune subdesarrollado, aumentando el riesgo de enfermedades causadas por patógenos por culpa de un sistema inmunológico inapropiado (Macpherson et al., 2004). No es realista disponer de animales libres de gérmenes, pero está claro que no todos los microbios son iguales en su capacidad para regular la respuesta inmune y proteger al hospedador de la enfermedad. Se ha llevado a cabo un estudio en ratones criados de forma convencional en el que fue suficiente con transferir microbiota de animales resistentes a infecciones entéricas a animales letalmente susceptibles para dotarlos de resistencia a la infección (Willing et al., 2011). Pese a que este tipo de estudios no se han llevado a cabo en cerdos, se ha demostrado que, antes de la infección, puede diferenciarse la microbiota de los cerdos que excretarán cantidades altas o bajas de Salmonella (Bearson et al., 2013). Además, al criar cerdos en un ambiente limpio con y sin exposición a la microbiota de un adulto se produjeron cambios en el desarrollo inmune así como en la capacidad para tolerar la infección por Mycoplasma hyopneumoniae (Schachtschneider et al., 2013).
Adquiriendo los microbios correctos
Como resultado de la co-evolución, los microbios intestinales benefician a su hospedador protegiéndolo de las enfermedades. Para destacar la importancia de la especificidad de hospedador y la co-evolución, se demostró que las cepas de un simbionte intestinal ubicuo de vertebrados, Lactobacillus reuteri, se agrupan en distintos clados en humanos, aves de corral, cerdos y roedores (Spinler et al., 2014). Hay que destacar que el sistema inmune es mucho menos robusto al responder a la colonización por microbios de una especie animal diferente (Chung et al., 2012). En la población humana hay un creciente reconocimiento de una "desaparición del microbioma" debido a cambios en nuestro comportamiento, en especial por lo que respecta a higiene y uso antibiótico, lo que conlleva un aumento de la incidencia de enfermedades inmuno-mediadas (Martínez et al., 2015; Blaser et al., 2009). De un modo parecido a lo que sucede en occidente con el aumento de la higiene, los sistemas intensivos de cría de ganado utilizan unas enérgicas medidas higiénicas y de bioseguridad para minimizar la exposición a patógenos. Un estudio reciente comparó el microbioma de cerdos domésticos y salvajes y encontró diferencias en la composición, especialmente en lo que respecta a Bifidobacterium (Ushida et al., 2015). ¿Cómo podemos esperar que nuestro ganado adquiera un microbioma sano si hay una exposición tan limitada a los microbios con los que han evolucionado?
La cría de lechones en unas condiciones de higiene excesiva promueve la activación del sistema inmune innato, sugiriendo una alteración de la homeostasis inmunológica (Mulder et al., 2011). Además, la proporción del simbionte Lactobacillus spp. aumenta cuando los cerdos son criados al aire libre, respecto a si son criados dentro de naves. Estos últimos tienen más filotipos potencialmente patógenicos de proteobacterias (Mulder et al., 2011; Mulder et al., 2009). Tal como muestra la figura 1, la higiene utilizada en la cría intensiva puede reducir la capacidad de formar una microflora estable, impidiendo un desarrollo y una función inmune normales, y aumentando potencialmente el riesgo de una enfermedad patogénica (Schmidt et al., 2011). Además de la exposición a los microbios adecuados, la investigación ha demostrado que el desarrollo de una comunidad microbiana estable en los cerdos requiere una exposición continuada al principio de su vida (Schmidt et al., 2011). Mientras se buscan las estrategias para aumentar la exposición a microbios co-evolucionados y promotores de la salud, es importante reconocer que la bioseguridad sigue siendo un factor crítico en la producción porcina.

Figura 1. Los cerdos expuestos a un ambiente con más microbios están más preparados para tolerar un desafío sanitario como resultado de una comunidad microbiana diversa y un sistema inmune más robusto.
Las consecuencias de los antibióticos: más allá de la resistencias
Los antibióticos han sido una herramienta clave para mantener la salud animal en la cría intensiva. Se utilizan para eliminar patógenos, pero representan uno de los factores que impactan sobre el desarrollo de una microbiota sana (figura 2) y, a veces, pueden favorecer la colonización por patógenos. Los tratamientos antibióticos en modelos experimentales han revelado que los microbios son necesarios para el mantenimiento de las defensas innatas de las mucosas (Willing et al., 2011). Se ha demostrado que dosis terapéuticas de antibióticos reducen la expresión de péptidos antimicrobianos y de genes de mucina, que son esenciales para evitar que los patógenos alcancen la superficie de la mucosa (Menendez et al., 1013; Wlodarska et al., 2011). Aunque apenas se ha estudiado el impacto de los antibióticos sobre las defensas innatas del cerdo, anecdóticamente los ganaderos encuentran un aumento de enfermedades tras un tratamiento antibiótico. También debe hacerse notar que los antibióticos pueden tener efectos a largo plazo sobre la composición y la función de la microbiota (Janczyk et al., 2007). He oído que algunos ganaderos echan un puñado de tierra en el corral cuando los lechones tienen diarrea. También es habitual administrar probióticos tras un tratamiento terapéutico con antibióticos. Estos productores van por el buen camino, sin embargo, se necesitan esfuerzos para desarrollar intervenciones más afinadas. Pese a que todavía hay muchas preguntas que necesitan respuesta, se está haciendo un esfuerzo en investigación para identificar las mejores poblaciones microbianas para el cerdo.
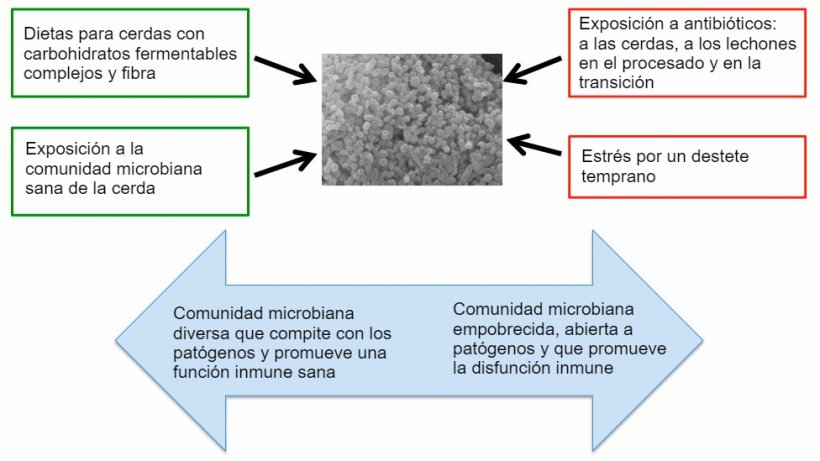
Figura 2. Factores que influencian sobre el desarrollo de un microbioma sano.



