Síndrome de dermatitis y nefropatía porcino
El síndrome de dermatitis y nefropatía porcino (SDNP) es una entidad clínico-patológica caracterizada por lesiones cutáneas y renales.

 |
 |
|
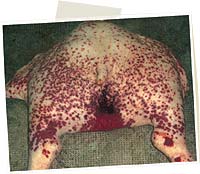
Cerdo de 4 meses con síndrome de dermatitis y nefropatía porcino. Nótese la presencia de manchas rojizas en el tercio posterior, las cuales tienden a coalescer en la zona perineal.
|
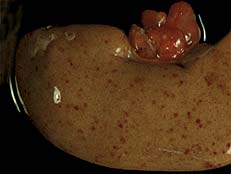
Riñón de cerdo afectado de síndrome de dermatitis y nefropatía porcino. Se trata de un riñón incremenado de tamaño, pálido y con petequias generalizadas. Nótese el marcado incremento de tamaño del linfonodo perirrenal.
|
La base patogénica de estas lesiones se atribuye a una reacción de hipersensibilidad tipo III. No obstante, actualmente se desconoce el presunto antígeno asociado a esta enfermedad.
Desde el punto de vista clínico-epidemiológico se destacan los siguientes aspectos del SDNP:
| Concepto | Características de la enfermedad |
| Edad de afectación | Transición y engorde (raramente adultos) |
| Morbilidad | 0,05 al 0,5% (esporádicamente hasta más del 20%) |
| Mortalidad | Próxima al 100% (menor cuanto más jóvenes) |
| Síntomas clínicos más habituales | Anorexia, depresión, postración, raramente hipertermia |
| Lesiones macroscópicas más representativas | Máculas y pápulas rojizo-negruzcas en la piel, especialmente en el tercio posterior (puede ser generalizado). Riñones incrementados de tamaño, blandos y con petequias generalizadas. |
| Lesiones microscópicas | Glomerulitis fibrinosa con nefritis intersticial. Vasculitis necrotizante sistémica. |
| Bioquímica clínica | Niveles incrementados de urea y creatinina |
| Causa de muerte | Coma urémico debido a un fallo renal agudo |
Actualmente se acepta que el diagnóstico del SDNP depende del cumplimiento de dos criterios básicos:
1. Presencia de lesiones hemorrágico-necrotizantes en la piel, especialmente en área perineal y en extremidades posteriores, y riñones blandos, pálidos con petequias generalizadas.
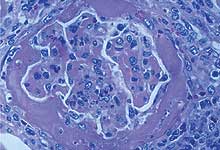
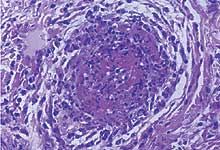
2. Presencia de vasculitis necrotizante sistémica y glomerulonefritis fibrino-necrotizante.
|
|||
|
Cerdo afectado de síndrome de dermatitis y nefropatía porcino. La glomerulitis fibrinosa (izquierda) y la vasculitis necrotizante (derecha) son los hallazgos histopatológicos característicos de esta enfermedad.
|
|||
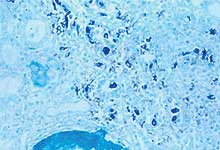 |
"Hibridación in situ" para la detección de genoma de PCV2 en el riñón de un cerdo afectado de síndrome de dermatitis y nefropatía porcino. Las células coloreadas en azul corresponden básicamente a macrófagos que contienen ácido nucleico de PCV2.
|
||
Como se puede observar, los criterios diagnósticos actuales no incluyen la infección por PCV2. Ello es debido a que no se ha demostrado de forma efectiva que PCV2 se encuentre implicado patogénicamente en el SDNP. De hecho, existen una serie de evidencias circunstanciales que asocian el virus a esta enfermedad:
• El SDNP se ha descrito aparentemente en los mismos países y regiones donde se ha descrito también la circovirosis porcina.
• Con gran frecuencia, los casos de SDNP se encuentran en granjas que sufren circovirosis porcina.
• Un porcentaje elevado de cerdos con SDNP sufren lesiones linfoides muy similares a las de la circovirosis porcina, aunque más leves.
• Un muy elevado porcentaje de cerdos con SDNP se encuentran infectados con PCV2, aunque con cantidades similares a los cerdos subclínicamente infectados con PCV2 (y, por tanto, mucha menor cantidad que los cerdos afectados con circovirosis porcina).
 |
|
Cerdo afectado con síndrome de dermatitis y nefropatía porcino. |
Los cerdos con SDNP presentan un título de anticuerpos frente a PCV2 significativamente mayor que cerdos sin esta enfermedad (sufran de circovirosis porcina o sean animales sanos).
Aunque existen una serie de elementos circunstanciales que asocian PCV2 y SDNP, actualmente no se ha demostrado fehacientemente una relación causal del agente con la enfermedad.
La importancia del SDNP es relativamente limitada dado que la prevalencia de la enfermedad en granja suele ser bastante baja.
¿Se puede controlar o prevenir la aparición del SDNP?
El desconocimiento de los factores desencadenantes del SDNP impide sugerir posibles estrategias de control y prevención frente a esta enfermedad.
En algunos casos se ha sugerido que el uso de antiinflamatorios inyectables podría ser beneficioso, dado que los cerdos que sufren de SDNP presentan un cuadro inflamatorio sistémico importante.
Enfermedad reproductiva
PCV2 se ha asociado a fallo reproductivo caracterizado por abortos tardíos y nacidos muertos, sea en presencia o ausencia de otros patógenos reproductivos bien establecidos.
Prácticamente todas las descripciones de estos fallos reproductivos se han realizado en Norteamérica.
Aunque no se han establecido formalmente los criterios para el diagnóstico de la forma reproductiva asociada a la infección por PCV2, éstos deberían ser:
|
1. Ocurrencia de abortos tardíos y nacidos muertos, observándose en algunos casos hipertrofia cardíaca en el feto.
2. Presencia de lesiones cardíacas caracterizadas por una miocarditis fibrosante y necrotizante en el feto. 3. Presencia de una elevada cantidad de PCV2 en las lesiones miocárdicas y otros tejidos fetales. |
 |
 |
|
(Foto cedida por el Dr. John A. Ellis, University of Saskatchewan, Canadá).
Pulmones y miocardio (centro) de fetos infectados intrauterinamente con PCV2. El miocardio presenta áreas de decoloración (necrosis) e hipertrofia. |
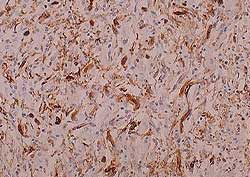
(Foto cedida por el Dr. John A. Ellis, University of Saskatchewan, Canadá).
Miocardio fetal en caso de fallo reproductivo asociado a la infección por PCV2. Nótese la masiva presencia de antígeno de PCV2 en el tejido miocárdico (coloración marronácea). Inmunohistoquímica. |
La frecuencia de estas alteraciones reproductivas en condiciones de campo es muy baja, y ello se asocia a la existencia de una alta prevalencia serológica frente a PCV2 en cerdas gestantes.
Complejo respiratorio porcino
El complejo respiratorio porcino (CRP) es una entidad clínica caracterizada por alteraciones respiratorias, retraso en el crecimiento, incremento del índice de conversión, e incremento de la mortalidad en cerdos de transición y/o engorde.
Desde el punto de vista etiológico se han asociado múltiples agentes infecciosos con la ocurrencia de CRP. Entre ellos se destacan:
|
- Virus del síndrome respiratorio y reproductivo porcino (PRRSV).
- Circovirus porcino tipo 2 (PCV2). - Virus de la enfermedad de Aujeszky (ADV). - Virus de la influenza porcina (SIV). - Coronavirus respiratorio porcino (PRCV). - Mycoplasma hyopneumoniae. - Actinobacillus pleuropneumoniae. - Pasteurella multocida. - Bordetella bronchiseptica. - Haemophilus parasuis. - Streptococcus suis. |
 |
Generalmente se consideran al PRRSV y Mycoplasma hyopneumoniae como los mayores contribuyentes al CRP. PCV2 debe considerarse como un agente infeccioso más a incluir en la lista de agentes que se asocian al CRP. PCV2 es capaz de generar también lesiones pulmonares, las cuales son, mayoritariamente, indistinguibles de aquellas inducidas por el PRRSV u otros virus. No obstante, además de la neumonía intersticial, también se ha asociado PCV2 a lesiones de bronquiolitis fibrosa. |
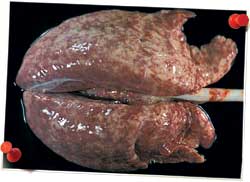
| Pulmón de un cerdo de 4 meses afectado de complejo respiratorio porcino. El patrón lobulillar observado conjuntamente con la ausencia de colapso pulmonar son indicativos de neumonía intersticial. Este hallazgo sugiere una infección vírica pulmonar y/o sistémica. | |
 |
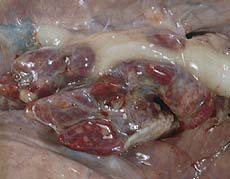 |
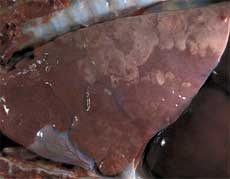
| Pulmón de un cerdo de 3 meses afectado de complejo respiratorio porcino. Marcada consolidación pulmonar craneo-ventral, indicativo de una infección bacteriana y/o micoplásmica. La ausencia de colapso pulmonar es indicativa de neumonía intersticial. | Pulmón de un cerdo de 4 meses afectado de complejo respiratorio porcino. Moderado a marcado incremento de tamaño de los linfonodos mediastínicos. |
Neumonía proliferativa necrotizante
La neumonía proliferativa necrotizante (NPN) se caracteriza patológicamente por:
|
• Presencia de células inflamatorias necróticas en el interior de los alvéolos.
• Presencia de macrófagos y material proteináceo en los alvéolos. • Presencia de hiperplasia de neumocitos de tipo 2. • Presencia de bronquiolitis necrotizante. • Presencia frecuente de incremento de grosor de los tabiques interalveolares debido a la acumulación de células inflamatorias mononucleares. |
 |
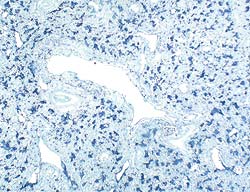 |
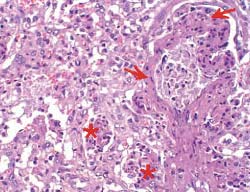
| Pulmón de cerdo de 4 meses con una neumonía proliferativa necrotizante. Nótese la necrosis del epitelio bronquiolar (flecha) y la presencia de células necróticas en los alveolos (asteriscos). Tinción de HE. | Pulmón de un cerdo de 4 meses con una neumonía proliferativa necrotizante. Masiva presencia de genoma de PCV2 (coloración azul). Hibridación in situ. |
La etiología de la NPN no ha sido del todo bien establecida, pero en un porcentaje muy elevado de casos se observa co-infección entre el PRRSV y PCV2.
Temblor congénito (mioclonia congénita)
El temblor congénito se caracteriza clínicamente por temblores generalizados de la cabeza y extremidades de lechones recién nacidos.
En el cerdo se describen dos grandes grupos de temblor congénito (uno de los cuales se subdivide en varios subtipos):
Temblor congénito tipo A: caracterizado por la presencia de lesiones microscópicas de desmielinización del sistema nervioso central y periférico:
|
→ Subtipo AI: asociado a la infección intrauterina por el virus de la peste porcina clásica.
→ Subtipo AII: asociado, presuntamente, a la infección intrauterina por un virus desconocido. Se ha postulado que PCV2 podría ser este virus. → Subtipo AIII: asociado a una condición hereditaria que afecta a machos de la raza Landrace. → Subtipo AIV: asociado a una condición hereditaria que afecta a lechones de ambos sexos de la raza British Saddleback. → Subtipo AV: asociado a la intoxicación intrauterina por un organofosforado. |
 Temblor congénito tipo B: caracterizado por la ausencia de lesiones microscópicas de desmielinización del sistema nervioso central y periférico.
Temblor congénito tipo B: caracterizado por la ausencia de lesiones microscópicas de desmielinización del sistema nervioso central y periférico.
Aunque inicialmente se asoció el temblor congénito AII a PCV2, las investigaciones más recientes indicarían que PCV2 no se encuentra relacionado con esta entidad clínica.