Caso clínico: Con ellas llegó el escándalo
04-may-2018 (hace 8 años 20 días)
Nos encontramos con una granja de 2000 reproductoras con un sistema de producción en tres fases. La reposición viene de una multiplicadora propia y disponen de recrías externas para el crecimiento de las futuras reproductoras desde los 20 hasta los 100 kg tras lo cual son introducidas en la granja. En estas recrías, efectuamos gran parte del programa sanitario y la monitorización antes de que entren en la explotación de producción. La granja de producción de lechones a 6 kg es positiva y estable a PRRS, y negativa a disentería, sarna y rinitis.
El programa de selección se basa en los siguientes puntos:
- Programa de selección de nulíparas
- Todas aquellas con un peso inferior a 1 kg al nacimiento son eliminadas como futuras reproductoras.
- Antes de enviarlas a las recrías con 20 kg se realiza otra selección, valorando la integridad de aplomos, línea mamaria y evolución general.
- En las recrías, y antes de entrar en granja, se verifican los aplomos, mamas y desarrollo genital.
- Programa sanitario de la reposición.
- Al destete se vacunan las híbridas, junto con los machitos, con PCV2 y micoplasma.
- En el periodo de recría que abarca desde los 20 hasta los 100 kg, se aplican las siguientes vacunas:
- Vacuna a las 10 semanas aproximadas y revacuna con 4 semanas de intervalo:
- Aujeszky e influenza.
- Vacuna viva de PRRS.
- Circovirus y Micoplasma. Esta vacuna es importante ya que, desde que se efectúa la vacunación masiva de PCV2, se ha reducido de manera notable la excreción del virus y entran al final del periodo de recría muchas nulíparas negativas a este virus. Antes de la vacuna en lechones, todos los animales al final del periodo de cebo eran positivos a circovirus.
- A las 27 semanas de vida: vacuna inactivada de PRRS.
- A las 29 semanas de vida y revacuna a las 4 semanas: vacuna de parvovirus y mal rojo.
- Vacuna a las 10 semanas aproximadas y revacuna con 4 semanas de intervalo:
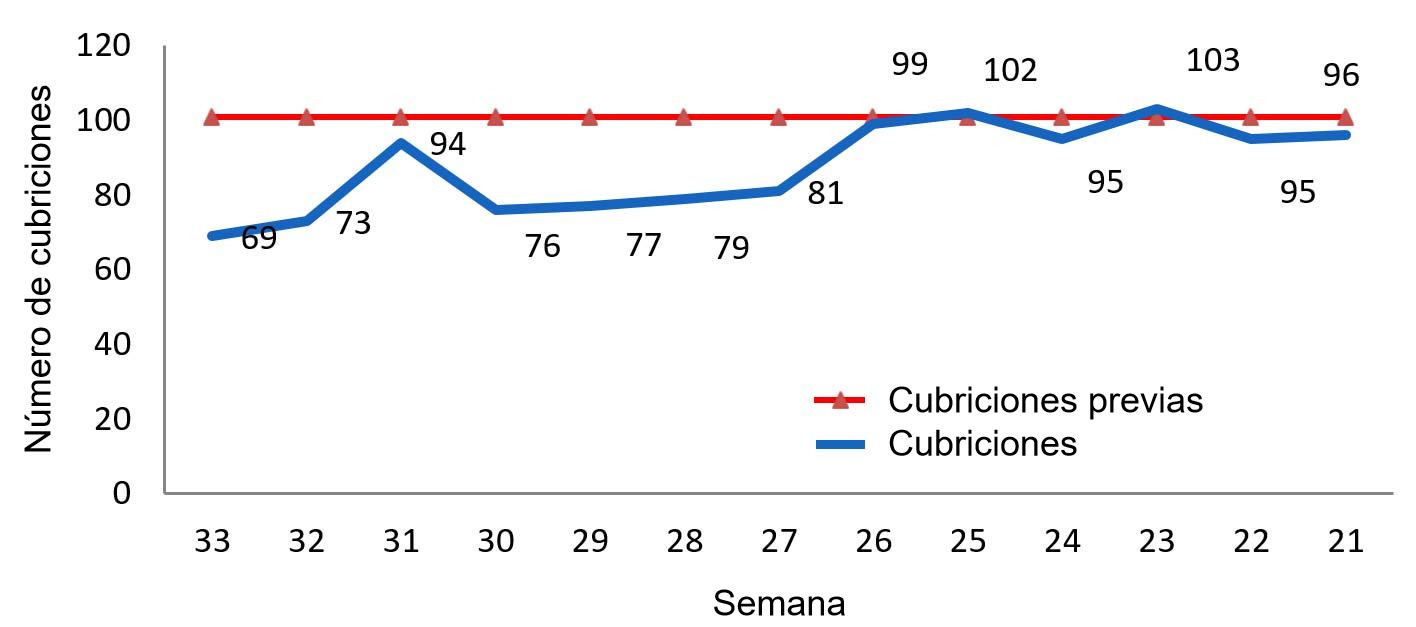
La idea es terminar el programa vacunal con 36-38 semanas de vida, un mes antes de su entrada en la zona de cubrición. Por diferentes motivos sanitarios, se decidió parar la entrada de este origen y por lo tanto nos encontramos sin nulíparas para poder cubrir (gráfico 1). Las consecuencias de este paso fueron:
- Caída del número de cubriciones semanales por falta de nulíparas.
- Se redujo el desvieje para intentar mantener el objetivo de cubriciones: se mantuvieron cerdas que en otras ocasiones se hubieran eliminado.
- El aumento de cerdas con más de 7 partos hizo que aumentara la variabilidad en la prolificidad y en la calidad de los lechones (las cerdas tienen peor producción y mayores gastos en alimentación).
Para alcanzar el objetivo de cubriciones, se decidió la compra de nulíparas de una fuente externa. Se introdujeron nulíparas con 100 kg, con un estatus sanitario superior al de la granja y mejores indicadores técnicos de prolificidad.
Estas primerizas entraron en una zona alejada, y se inició el programa de adaptación, que era en esencia el que se venía aplicando de manera rutinaria a las nulíparas del multiplicador propio, pero, para reducir el tiempo de adaptación, se procedió a combinar vacunaciones con tres semanas de intervalo entre vacuna y revacuna.
Eficiencia de las nulíparas externas
La eficiencia reproductiva del lote fue buena. Se eliminaron menos del 2% de las nulíparas entradas y las repeticiones fueron inferiores al 6%. En partos tuvieron un mayor número de lechones nacidos totales (subida de 1,2 lechones). Como es normal, y ya esperado, el peso al nacimiento de los lechones fue menor y la variabilidad de pesos se incrementó.
Inicio del proceso patológico en la explotación
En los partos de las primerizas, en los primeros días tras el nacimiento, se produjo un proceso de diarrea en los lechones que ocasionó una pérdida de condición corporal importante (foto 1). Los tratamientos con antibióticos no corrigieron la clínica, aunque redujeron la gravedad del proceso y la mortalidad de los lechones. Es decir, hubo un aumento de los lechones que sufrieron una pérdida de peso y que terminaron por morirse o generaron un aumento notable del número de lechones retrasados.

La diarrea y el retraso generaron una pérdida del desarrollo mamaria de las cerdas, al producirse un vaciado parcial de la leche de la glándula mamaria (foto 2).
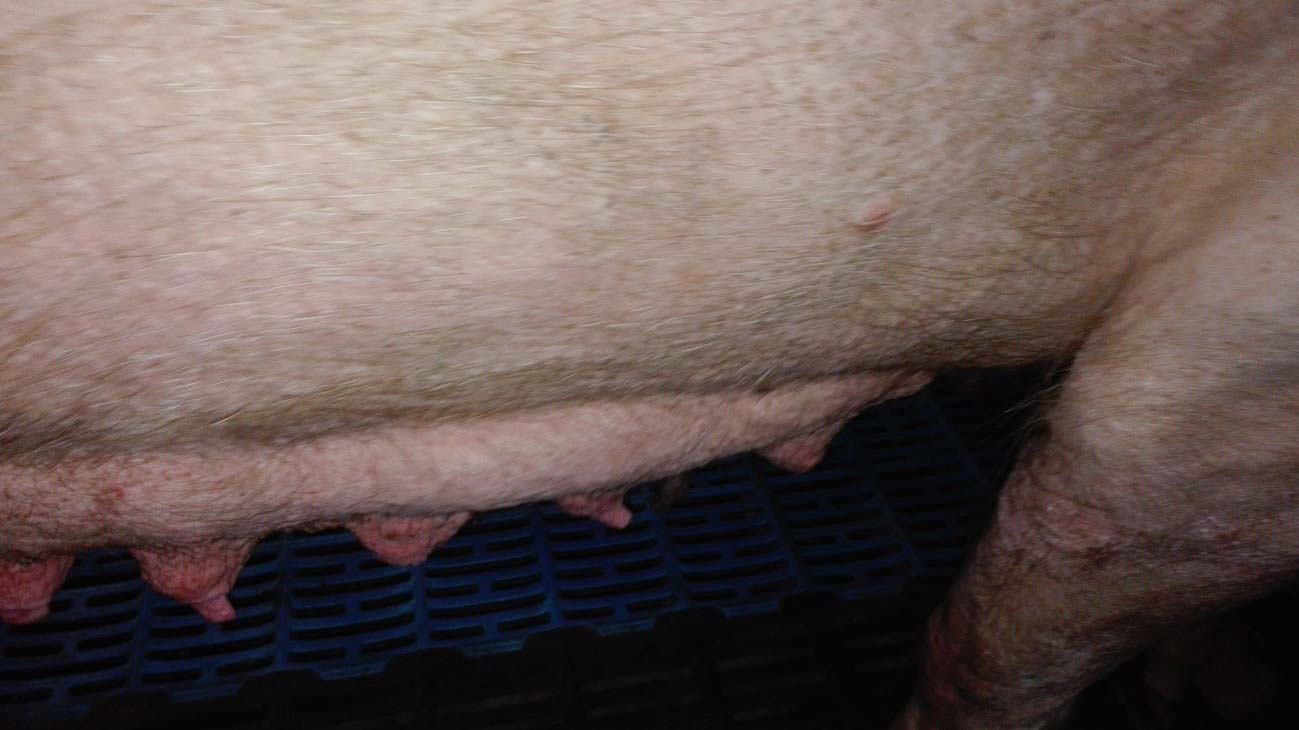
La pérdida de calidad de los lechones se reflejó en la transición, generándose mayor número de colas por la baja calidad de los lechones al destete.
Abordaje del diagnóstico
Se valoraron las condiciones ambientales y de alojamiento y posteriormente se revisó el manejo de los animales.
Utilizamos una lista de chequeo básica, la cual nos informa de las posibles causas de diarrea que tengan un origen en el manejo de la paridera (tabla 1)
Tabla 1: Lista de chequeo en partos.
| Condiciones de riesgo |
Efecto | Condiciones óptimas | Efecto | ||
| Ambiente | Temperatura de la sala | >28ºC <14ºC | • ↓ consumo pienso y producción láctea • Alteración bienestar |
Termoneutralidad de la cerda (18-22ºC) sin corrientes de aire | • ↑ consumo pienso lactación • ↑ leche |
| Temperatura de la placa | Frío | Aplastamientos | • Papel secante • Placa caliente • 36-38ºC • Bombilla extra • Secado rápido |
• Descanso en placa • ↓aplastados |
|
| Alimentación reproductora | Bebederos cerda | Caudales inferiores a 2 L/m | • ↓ producción láctea • ↓ calidad fisicoquímica y microbiológica agua |
• >2 L/m • Agua limpia y fresca • Bebederos de nivel • Suplementación |
• ↑ consumo pienso lactación • ↑ leche |
| Comederos cerda | Sucios Restos fermentaciones |
• Limpieza • Accesibilidad |
|||
| Curva alimentación | Alimentación inadecuada a mitad de gestación y final | Posible edema mamario |
Revisar niveles gestación y lactación |
↑ producción de calostro y leche al inicio de lactación | |
| Pienso | Tipos y consumos | ||||
| Vacío sanitario, limpieza y desinfección | Vacío sanitario | <3 días vacío Humedad |
• ↑ presión de infección • Presencia de diarreas |
• Secado • >3 días |
↓ de la presión de infección |
| Limpieza y desinfección | Ausencia de limpieza y desinfección | • Detergente • Limpieza fosos • Rotación desinfectantes |
Se mandaron muestras al laboratorio, torundas rectales y contenido de paquetes intestinales (tabla 2) de lechones no medicados. Se solicitaron PCR para coronavirus, rotavirus y factores de virulencia de E. coli. Si en esta primera aproximación no se conseguían datos concluyentes, se iba a proceder a la realización de histopatología.
Tabla 2: Resultados de las muestras de contenido intestinal
| Identifiación muestra | Nutri pool heces |
| Rotavirus A | + |
| Gastroenteritis Transmisible (TGEV) | - |
| Diarrea Epidémica Porcina (PEDV) | - |
En las torundas (tabla 3) apareció un E. coli sin factores de virulencia, que casi con toda probabilidad complicaba el cuadro clínico de los lechones y originaba mayor mortalidad.
Tabla 3: Resultados de las muestras de las torundas
| Cepa | Adesinas | Toxinas | |||||||
| F4 (K88) | F5 (K99) | F41 | F6 (987P) | F18 | LTI | ST-Ia | ST-II | Stx2 | |
| E. coli spp | - | - | - | - | - | - | - | - | - |
| E. coli spp | - | - | - | - | - | - | - | - | - |
| E. coli spp | - | - | - | - | - | - | - | - | - |
En las necropsias solo se apreció el intestino traslúcido, lo que hacía sospechar una pérdida importante de las vellosidades intestinales. Rotavirus, provoca una destrucción de los enterocitos maduros, su lugar de replicación. La proliferación de enterocitos inmaduros da lugar a diarrea debido a su actividad secretora. En algún animal también se observó cierta congestión del intestino y diarrea amarillenta.
El uso de antibióticos para el tratamiento de estas diarreas en la que el agente iniciador es un virus y después se complica con bacterias, da lugar a variaciones importantes de la microbiota del lechón y su integridad intestinal, lo que impide su correcto desarrollo (foto 3).

Abordaje terapéutico
En primer lugar, se puede usar la retroalimentación con heces de animales afectados dándoselos a las nulíparas gestantes un mes antes del parto. Esta medida suele aportar buenos resultados, aunque presenta algunos inconvenientes y tiene un riesgo sanitario muy importante. Los inconvenientes con los que nos encontramos a la hora de realizar esta práctica son:
- Es fundamental inactivar el cloro del agua en el que ponemos las heces con leche o tiosulfato;
- En ocasiones no hay suficiente diarrea para recoger con fregona y se añaden paquetes intestinales. En granjas positivas a PRRS es un riesgo importante (aunque sean estables siempre hay un % de animales que pueden estar virémicos)
- No se debe emplear material procedente de lechones de más de 5 días. Después de este plazo, podemos inmunizar contra rotavirus, ya que es muy ubicuo y se necesita una baja dosis infectiva pero es posible la transmisión de otras patologías presentes en la granja.
Por todos estos inconvenientes, somos de la opinión de no usar ni recomendar la retroalimentación con heces.
En nuestro caso, las actuaciones para solucionar este problema fueron:
- Como disponíamos de una vacuna contra colibacilosis y toxoide de Clostridium perfringens tipo C (que contiene rotavirus A virus vivo atenuado), efectuamos la vacunación de las nulíparas gestantes a los 60 y los 90 días de gestación. El objetivo fue obtener una alta concentración de anticuerpos en calostro. El calostro no deja de ser un reflejo del historial inmunitario de la cerda.
La vacunación, en estos casos, es la alternativa terapéutica más segura y eficaz, aunque hay que asegurar una inmunidad pasiva de los lechones vía calostro. - Monitorización del encalostramiento de los lechones, comprobando que los animales de menos peso, y los que habían podido sufrir algo de estrés térmico o estrés en el parto, tomasen calostro en las primeras horas tras el nacimiento. Calor adicional y papel para que los lechones se sequen rápidamente, son alternativas útiles para incrementar la vitalidad de los lechones.
- La monitorización de la higiene y la alimentación de la cerda en el periodo de transición entre los últimos días de gestación y los primeros días de lactación es básica para evitar un edema mamario e hipogalaxia (foto 4). En estos dos casos, se da lugar a un proceso clínico por deficiencias en la producción de calostro. Hay que tener especial cuidado con la cantidad del incremento de pienso en el último tercio de la gestación y el periodo de periparto: puesto que no sólo se pueden dar fallos en la producción de calostro, sino que, además, puede dar fallos en la producción láctea de la cerda después del parto.
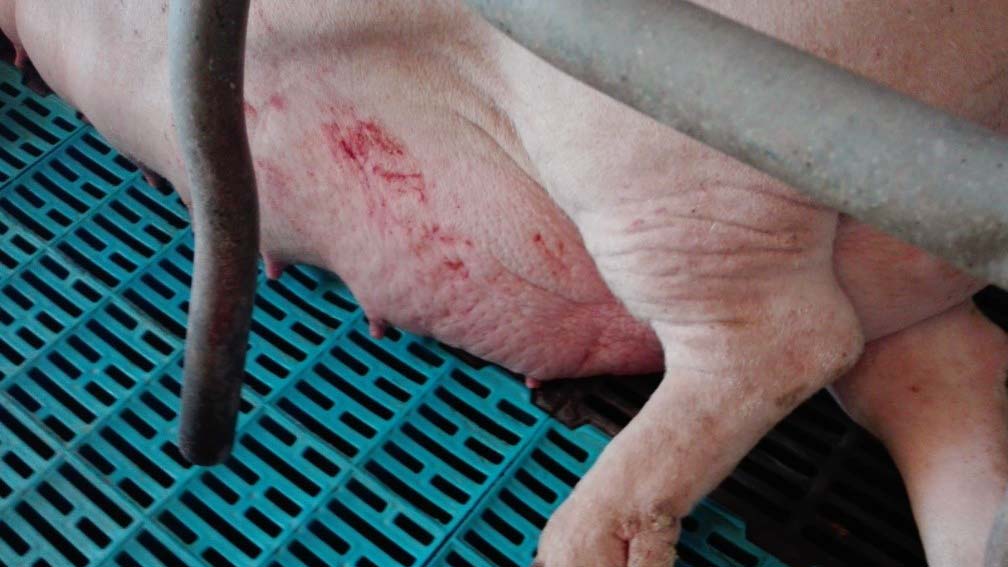
- Como es lógico, se mantuvieron las medidas de higiene estricta en la paridera para disminuir la presión de infección. La limpieza de la paridera con espuma, con objeto de limitar la carga vírica en los laterales de la rejilla de los lechones, es fundamental. El uso de espuma facilita que el desinfectante llegue a todos los rincones del piso de rejilla. La limpieza tiene que ser efectuada en profundidad, intentando limpiar los fosos de purines y bañando a las cerdas a su entrada en paridera. Las cerdas y el suelo se deben dejar secar antes de los partos tras aplicar la espuma con clorhexidina.
- Hay que observar la vitalidad de los animales en el parto ya que de ella depende que el encalostramiento sea mejor o peor. Es básico vigilar la temperatura de la cerda y la duración parto.
Conclusiones
- Desconocemos si el rotavirus estaba en la granja o lo traían las nulíparas que venían de fuera, lo cierto es que el proceso entérico debido a rotavirus, con las infecciones secundarias por colibacilos, agravó el proceso clínico y aumentó los días de curación clínica, lo que empeoró el estado de los lechones al destete e incrementó la mortalidad y la pérdida de producción lechera.
- Los cambios en el origen sanitario de las futuras reproductoras son siempre decisiones difíciles. No es suficiente con la monitorización, mediante analíticas, antes de la introducción de los animales nuevos a la explotación.
- Los procesos entéricos en lactación tienen mayor incidencia cada día. Es necesario apoyarnos más en el uso de la vacunación, en las medidas de manejo de los animales y en los protocolos de limpieza y desinfección de las parideras y cerdas para bajar la presión de infección: este debe ser nuestro gran objetivo.
- La vacunación por sí sola no es garantía de éxito si no se controla el encalostramiento correcto de los lechones y se maneja precozmente cualquier incidencia que repercuta en calostro producido y en la cantidad de calostro ingerido por los lechones. Una vez corregidas todas las contingencias del manejo, el uso de las vacunas nos ayudarán al éxito.
El incremento en la prolificidad que se ha producido en los últimos años hace que se haya reducido la ingesta de calostro por individuo: un menor peso al nacimiento hace que estos tengan menos vitalidad, y por lo tanto, menor capacidad de una buena ingesta de calostro.
