Influenza und PRRSV: Gemeinsamkeiten, Unterschiede und Wechselwirkungen
23-Feb-2026 (vor 3 Monate 15 Tage)
Das PRRSV und das Influenzavirus gehören unterschiedlichen Virusfamilien mit unterschiedlichen Pathogenitätsmechanismen an, weisen jedoch einige gemeinsame Merkmale auf:
- Hohe genetische Diversität: Beide Viren weisen eine sehr hohe Mutationsrate auf und beide besitzen die Fähigkeit, Teile bzw. Segmente ihres Genoms auszutauschen, auch wenn sie dies auf unterschiedliche Weise tun.
- Hohe Verbreitung: > 70 % der spanischen Betriebe sind für beide Erreger positiv.
- Fähigkeit zur endemischen Etablierung im Betrieb:
- IAV: Die endemische Form entsteht durch das Vorhandensein von Subpopulationen mit unterschiedlichen Immunitätsniveaus im Bestand. Die unterschiedliche Immunerfahrung von jungen und älteren Sauen kann das Auftreten von Infektionen im Abferkelstall beeinflussen, wobei Ferkel von Jungsauen eine höhere Wahrscheinlichkeit haben, sich zu infizieren. Diese frühe Übertragung erfolgt in der Regel horizontal – zwischen Würfen oder auch über unbelebte Infektionsträger (Fomiten). Es wurde eine Serokonversion bei Sauen während der Laktationsphase beschrieben, was darauf hindeutet, dass Ferkel eine Infektionsquelle für Sauen darstellen können. Am häufigsten infizieren sich Ferkel jedoch in der Aufzuchtphase, wenn die maternalen Antikörper abnehmen. In betroffenen Aufzuchtstationen wird typischerweise eine erhöhte IAV-Inzidenz beobachtet, verbunden mit einer Zunahme klinischer Parameter (Niesen, Husten und tiefsitzender Husten).
- PRRS: Die vertikale Übertragung ist häufig, und die Geburt virämischer Ferkel trägt maßgeblich zur Aufrechterhaltung des Infektionszyklus im Betrieb bei. Je höher die Anzahl virämisch geborener Ferkel, desto stärker ist die horizontale Übertragung während der Aufzuchtphase.
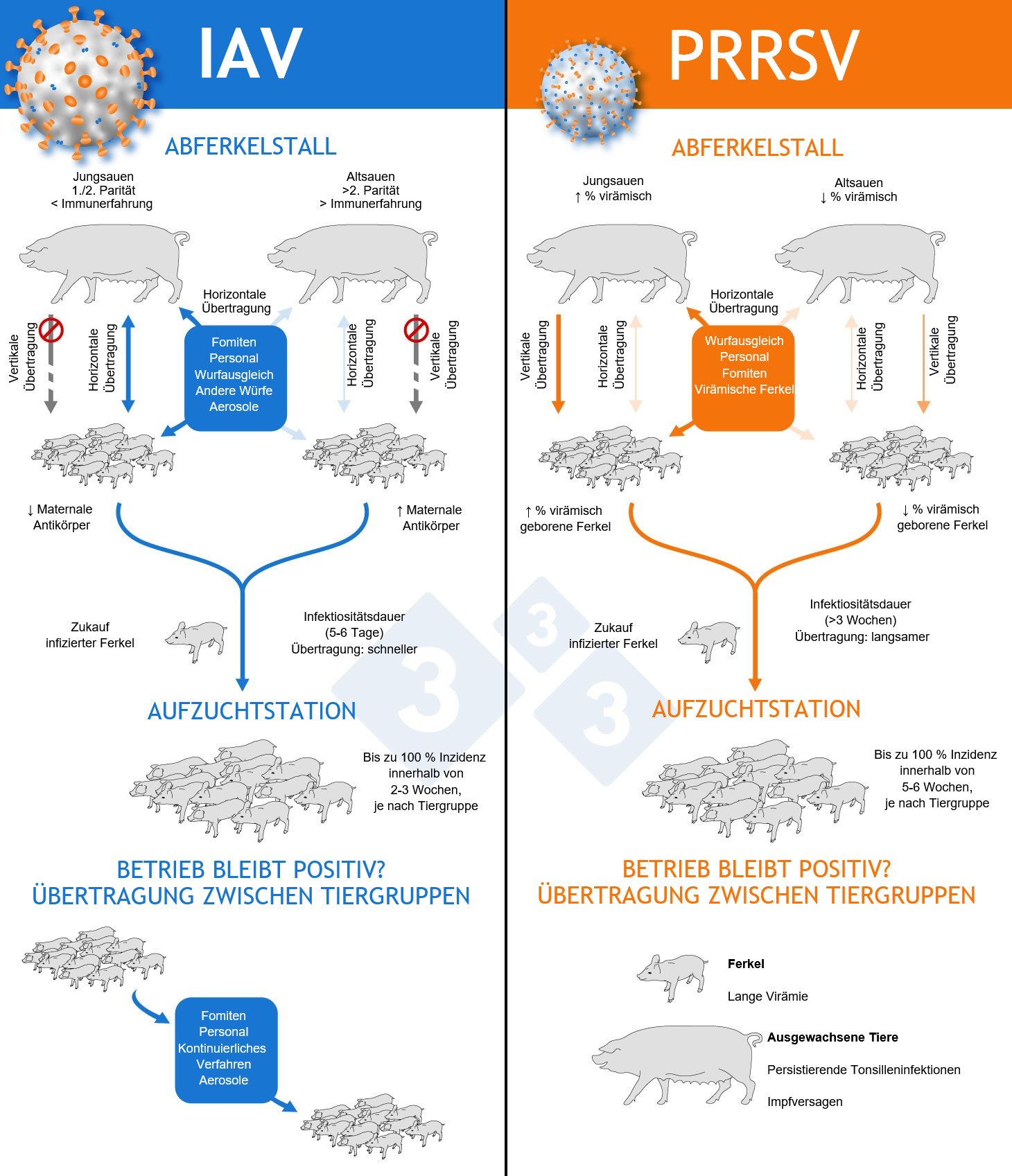
In ihren endemischen Verlaufsformen weisen beide Viren im Durchschnitt ähnliche Übertragungsraten (R₀-Werte zwischen 2 und 7) auf, unterscheiden sich jedoch hinsichtlich der Dauer der Ansteckungsfähigkeit:
- Beim PRRSV ist sie deutlich länger (>3 Wochen bei Ferkeln).
- Beim IAV ist sie kürzer (durchschnittlich 5-7 Tage), weshalb die Übertragung schneller erfolgt. Selbst unter endemischen Bedingungen können epidemische Übertragungsmuster beobachtet werden, wobei in bestimmten Buchten oder Tiergruppen von einem einzelnen Indexfall ausgehend mehr als 10 Neuinfektionen auftreten können – etwas, das beim PRRSV unter endemischen Bedingungen nur selten beobachtet wird.
Interaktion mit anderen Krankheitserregern: unterschiedliche Wirkmechanismen
Ein weiterer gemeinsamer Aspekt ist die Zunahme bakterieller Sekundärinfektionen. Allerdings unterscheiden sich auch hier die zugrunde liegenden Mechanismen:
- IAV: Das Virus verursacht eine Zerstörung des zilientragenden Epithels sowie eine sehr ausgeprägte Entzündungsreaktion im Respirationstrakt. Dadurch wird die Besiedlung durch bakterielle Erreger begünstigt, die bis in die Lunge vordringen können, was die Häufigkeit sekundärer bakterieller Pneumonien erhöht.
Es wurden klare synergistische Effekte zwischen IAV und Mycoplasma hyopneumoniae sowie mit Actinobacillus pleuropneumoniae beschrieben.
- PRRSV (konventionelle Stämme): Die Infektion beschränkt sich auf permissive Makrophagen, die in den oberen und mittleren Atemwegen nur in geringer Zahl vorkommen und sich hauptsächlich in den Alveolen sowie in den pulmonalen Gefäßen befinden. Die Entzündungsreaktion kann in der Lunge sehr ausgeprägt sein, tritt jedoch in anderen Geweben nicht wesentlich in Erscheinung. Die mit der Primärinfektion durch PRRSV assoziierte respiratorische Klinik ist variabel, was jedoch nicht bedeutet, dass sie nicht erheblich sein kann. Je nach Virulenz des jeweiligen Stammes ist die Infektion mit einer Verschlechterung der Immunantwort sowie mit einer Depletion der alveolären Makrophagen verbunden. Dies erleichtert das Eindringen weiterer Bakterien und erhöht den Anteil bakterieller Pneumonien und systemischer Infektionen. Zudem wurden synergistische Effekte zwischen dem PRRSV und PCV2 beschrieben.
- PRRSV (hochvirulente Stämme): Bei hochvirulenten PRRSV-Stämmen ist die Entzündungsreaktion deutlich ausgeprägter und verursacht primär eine respiratorische Pathologie mit klarer klinischer Symptomatik, die von Beginn an mit Mortalität verbunden ist. Überleben die Tiere die Infektion, zeigen sie eine hohe Anfälligkeit für bakterielle Sekundärinfektionen über längere Zeiträume. Dies liegt daran, dass die Infektion mit einer Thymusatrophie sowie einer stark ausgeprägten Lymphopenie einhergeht.
Interaktion zwischen swIAV und PRRSV
Die Wechselwirkungen zwischen diesen beiden Viren sind komplex, und widersprüchliche Ergebnisse sind keine Seltenheit. In einer experimentellen Studie untersuchten Van Reeth et al. die Koinfektion mit PRRSV und IAV in zwei Tiergruppen. Während in einer Gruppe eine deutliche Synergie zwischen beiden Viren beobachtet wurde, zeigte die andere Gruppe ein milderes klinisches Bild, als es bei einer Einzelinfektion mit jeweils einem der beiden Viren zu erwarten gewesen wäre.
In einer neueren Studie (Martín-Valls et al., 2022) wurde das Vorkommen von elf respiratorischen Viren sowohl auf Einzeltier- als auch auf Bestandsebene untersucht, darunter IAV, PRRSV1, PCV2, das porzine Zytomegalovirus (PCMV), das porzine respiratorische Coronavirus (PRCV) und das porzine Orthopneumovirus (SOV). Die Ergebnisse auf Bestandsebene zeigten eine Assoziation zwischen IAV, PCMV und SOV, jedoch nicht mit PRRS-Viren. Auf Einzeltier-Ebene korrelierten IAV und PRRSV negativ miteinander. Diese negative Korrelation war zuvor auch in vitro beschrieben worden, in einer Studie, in der eine Replikationsinterferenz in koinfizierten CD163⁺-Zellen beobachtet wurde. In einer weiteren experimentellen In-vivo-Studie beeinträchtigte eine vorherige PRRSV-Infektion die nachfolgende IAV-Infektion ebenfalls negativ.
In einer neueren Studie, in der die gleichzeitige Zirkulation dieser beiden Viren in Schweinepopulationen longitudinal von der Geburt bis zum Ende der Absetzphase untersucht wurde, zeigte sich, dass das Vorhandensein eines hochvirulenten PRRS-Virus zu Folgendem führte:
- einer Zunahme der Zahl von Tieren, die wiederholt mit swIAV infiziert wurden,
- einer Verlängerung der Dauer der IAV-Infektion (in einigen Fällen über 2 Wochen hinaus). Dies könnte mit einer Verschlechterung der Immunantwort dieser Tiere in Zusammenhang stehen.
Die Auswirkungen auf die Produktion und die Tiergesundheit zu beurteilen, ist schwierig. Cornelison et al. verglichen zwei Betriebe, die mit PRRSV und IAV koinfiziert waren, mit einem Betrieb, der nur mit PRRSV infiziert war. Dabei beobachteten sie in den koinfizierten Betrieben eine bis zu 19 % höhere Mortalität sowie eine Verringerung der durchschnittlichen Tageszunahme (bis zum Schlachtalter) um 8 – 14 %.
Fazit
Die Beziehung zwischen diesen Viren ist komplex und kann in verschiedenen Studien widersprüchlich erscheinen. Das Auftreten hochpathogener PRRSV-Stämme sowie die hohe genetische Diversität beider Viren machen es sehr schwierig (wenn nicht gar unmöglich), die relativen Auswirkungen jedes Virus vorherzusagen. Auch wenn sie auf Einzeltier-Ebene offenbar nicht additiv wirken, ist ihr Einfluss sowohl einzeln als auch in Kombination auf Bestandsebene deutlich erkennbar.
