Die Auswirkungen des Problems der PRRSV-Rekombinationen
14-Jul-2025 (vor 10 Monate 28 Tage)
Rekombination ist ein natürliches Phänomen und eine Triebkraft der genetischen Evolution des PRRS-Virus. Seit den späten 1990er Jahren wird über das Auftreten von Rekombinationen in Laborexperimenten mit Zellkulturen berichtet. Damit ein Rekombinationsereignis stattfinden kann, müssen zwei Viren eine Zelle infizieren, sich replizieren und dabei genetisches Material austauschen, damit daraus ein neues Nachkommenvirus entsteht (s. Abb. 1).

In der neueren Literatur wird von Rekombinationen zwischen:
- Wildtyp-Viren (WT)
- Viren modifizierter Lebendimpfstoffe (MLV) sowie
- zwischen Wildtyp- und Impfviren berichtet.
Solche Rekombinationsereignisse sind in der Praxis möglicherweise schon immer aufgetreten. Was sich jedoch in den letzten Jahren geändert hat, ist unsere verbesserte Fähigkeit, diese Ereignisse durch den verstärkten Einsatz von Next-Generation-Sequencing (NGS) zu erkennen. Ein Beispiel hierfür ist der am 7. Juli 2025 auf www.pig333.com veröffentlichte Artikel „PRRS-Molekulardiagnostik: Wenn die Sequenzierung von nur 4 % nicht ausreicht“. Zudem stehen nun Bioinformatik-Tools für die Rekombinationsanalyse zur Verfügung.
Viele der in der Praxis auftretenden Rekombinationen bringen nicht lebensfähige Viren oder Viren hervor, denen es nicht gelingt, eine richtige Infektion auszulösen und in der Population zu überleben. Die größte Gefahr für die Tiergesundheit geht jedoch von Rekombinationen zwischen zwei verschiedenen Wildtyp-Viren aus (siehe Abb. 2).
Die kürzlich aufgetretenen Stämme Rosalia und L1C.5 sind Beispiele für aggressive rekombinante Wildtyp-PRRS-Viren. Sie haben sich endemisch in der Schweinepopulation etabliert und führen zu aggressiven klinischen Symptomen.
Es bleiben jedoch die folgenden Fragen:
- Warum gewinnt man den Eindruck, dass es mehr rekombinante PRRS-Viren gibt, die von Lebendimpfstoffviren abstammen?
- Was geschieht mit diesen neuen Viren?
Auf dem Etikett von modifizierten Lebendimpfstoffen wird deren Einsatz bei gesunden Tieren empfohlen, damit diese vor einer Infektion mit dem Wildtyp eine individuelle Immunität entwickeln können. Bei der Bekämpfung von PRRS-Wildtypen zirkulieren MLV-Impfviren häufig zusammen mit Wildtyp-Viren. Von modifizierten Lebendimpfstoffen stammende rekombinante Viren sind nicht so aggressiv wie Wildtyp-Viren oder Wildtyp-Rekombinanten (s. Abb. 2).
In den Vereinigten Staaten gibt es Fallberichte, die beschreiben, dass Maßnahmen wie verstärkte Biocontainment- und Biosicherheitsmaßnahmen zur Vermeidung der Ausbreitung des Virus in Abferkelställen sowie Maßnahmen zur Verbesserung der Immunität einzelner Ferkel vielversprechende Ergebnisse bei der Verringerung der klinischen Auswirkungen der neu aufgetretenen, von modifizierten Lebendimpfstoffen stammende PRRSV-2-Viren gezeigt haben. In Europa wurde ebenfalls berichtet, dass PRRSV-1-Rekombinanten, die von modifizierten Lebendimpfstoffen stammen, in klinischen Versuchen nicht so mild wie die MLV-Viren und auch nicht so aggressiv wie die Wildtyp-Viren sind.
Rekombinante, chimäre PRRSV-2-Viren, die im Labor aus Wildtyp- und MLV-Impfviren entstanden sind und Schweinen zu Versuchszwecken geimpft wurden, zeigen im Vergleich zu Wildtyp-Viren weniger aggressive klinische Anzeichen, jedoch keine so milden klinischen Auswirkungen wie die MLV-Elternviren (s. Abb. 2). Darüber hinaus gibt es Berichte, in denen rekombinante Wildtyp-Viren aus landwirtschaftlichen Betrieben, die aus MLV-Impfstoffen und Feldstämmen entstanden sind, zusätzliche Herausforderungen für das Wachstum in Zellkultur darstellten.
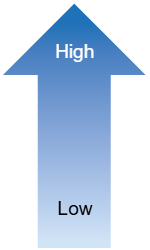
Abbildung 2: Klinische Auswirkungen und bioinformatische Möglichkeiten zum Nachweis von Rekombinationen zwischen verschiedenen PRRS-Viren.
| PRRSV-Stamm | Klinische Auswirkungen | Bioinformatische Möglichkeiten zum Nachweis von Rekombinationen |
|---|---|---|
| MLV (Modifiziertes Lebendvirus) | 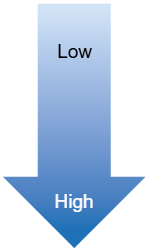 |
 |
| Rekombinantes MLV & MLV | ||
| Rekombinantes MLV und WT-PRRSV (Wildtyp-PRRSV) | ||
| WT-PRRSV | ||
| Rekombinantes WT-PRRSV und WT-PRRSV |
Ein weiterer Ansatz zur Bekämpfung von PRRSV, der in einigen Ländern verfolgt wird, ist die Verabreichung von Lebendvirusinokulum (LVI). Dabei werden Proben (z. B. Serum oder Lunge) direkt aus dem Betrieb entnommen. Das Vorhandensein von PRRSV wird durch RT-PCR bestätigt. Anschließend werden die Proben in einem Medium verdünnt und die Tiere dem im Betrieb vorhandenen Feldvirus ausgesetzt.
Im Gegensatz zu MLV sind Feldviren nicht abgeschwächt. Insbesondere LVI könnten unwissentlich mehrere PRRSV-Stämme enthalten, wodurch sich die Möglichkeit einer Wildtyp-Rekombination ergibt.
Darüber hinaus ist die Verwendung von LVI-Material in vielen Ländern gesetzlich nicht zugelassen. Zudem kann es andere Krankheitserreger enthalten, die im Blutkreislauf der Spender zirkulieren, beispielsweise das Porcine Circovirus oder das Porcine Parvovirus, was die Seuchenbekämpfung zusätzlich erschwert.
Welche Auswirkungen hat das Vorhandensein mehrerer und/oder rekombinanter Stämme von PRRS?
- In Zuchtbetrieben, die mit drei oder mehr Stämmen von PRRSV infiziert waren, gab es 1.837 mehr tote Ferkel pro 1.000 Sauen als in Betrieben, die mit maximal 2 Stämmen infiziert waren. Dies untermauert die Tatsache, dass die klinischen Auswirkungen bzw. Symptome umso größer sind, je mehr PRRSV-Stämme in der Population, im Bestand oder im Schwein zirkulieren (je mehr Stämme, desto schlimmer).
- Zuchtbetriebe, bei denen während der PRRSV-Eliminierung drei oder mehr PRRSV-Stämme nachgewiesen wurden, benötigten 12 Wochen länger, um die Stabilität zu erreichen, als Betriebe mit maximal 2 Stämmen.
- Betriebe, in denen zum Zeitpunkt des Ausbruchs ein rekombinantes PRRSV-Virus nachgewiesen wurde, hatten 1.827 tote Ferkel mehr pro 1.000 Sauen als Betriebe, in denen keine rekombinanten Stämme nachgewiesen wurden.
Die Bekämpfung von PRRS kann dazu beitragen, das Auftreten von Rekombinationsereignissen zu verringern.
Beispiele für solche Maßnahmen sind:
- Vermeiden Sie die Aufnahme von Jungsauen, die mit einem anderen PRRSV-Stamm infiziert sind als der, welcher derzeit im Zuchtbestand vorkommt.
- Vermischen Sie keine Ferkel und Mastschweine, die mit verschiedenen PRRSV-Wildtypen infiziert sind.
- Testen Sie LVI-Proben vor der Injektion mittels NGS und vermeiden Sie die Verwendung von LVI-Material, das mehrere genetisch unterschiedliche PRRSV-Stämme enthält.
- Wenn das LVI-Material ein MLV-ähnliches Virus enthält, verwenden Sie den modifizierten Lebendimpfstoff aus einem Impfstoff-Fläschchen anstelle eines Feldvirus.
- Vermeiden Sie es bei der Verwendung von MLV, zwei Lebendimpfstoffe zu mischen oder gleichzeitig zu injizieren. Vermeiden Sie auch den Wechsel von MLV-Impfstoffen innerhalb eines Betriebs oder einer Partie.
- Befolgen Sie die Empfehlungen auf dem Etikett des MLV-Impfstoffs, die auf den Einsatz bei gesunden Tieren hinweisen. Auf diese Weise induzieren Sie eine individuelle Immunität gegenüber der erwarteten Infektion mit einem Wildtyp.
PRRSV ist ein bereits jetzt schwieriger und die Tiergesundheit bedrohender Erreger, der sich im Laufe der Zeit genetisch weiterentwickelt. Eine erfolgreiche Bekämpfung von PRRSV führt nicht nur zu besseren Produktivitätsergebnissen, sondern verringert auch die Möglichkeiten für verschiedene Wildtyp-Viren, zu rekombinieren und noch aggressivere Viren hervorzubringen.
