Caso clínico: Infecção pulmonar poli-microbiana
Descrição da exploração
Trata-se de uma exploração de ciclo fechado com 600 porcas situada numa zona de França com baixa densidade porcina: a exploração conta com:
- Maneio semanal
- Desmame aos 21 dias (20 bandas)
- Fabrico do alimento na própria exploração
- Reposição própria
Origem das primíparas: Na exploração entram avós, a partir das quais se criam as fêmeas para reposição, as quais se separam dos animais de produção aos 18 kg.
Aos 180 dias transferem-se para uma quarentena onde permanecem até aos 250 dias após os quais são inseminadas numa sala de cobrição especial (35 lugares) e depois são transferidas para as salas de gestação.
Alojamentos:
| Varrascos | Cobrição | Gestantes | Maternidade |
| 6 varrascos em produção | 180 porcas alojadas em jaulas individuais |
180 porcas em jaulas individuais 170 porcas em grupos (grupos de 10) |
4 parques de 30 lugares |
| Transição | Crescimento | Engorda | |
|
4 parques de 280 lugares (ar filtrado) |
4 parques de 300 lugares (alimento seco) (construção antiga) |
19 parques de 280 lugares (alimentação líquida) (construção recente) |
|
A sucessão dos pavilhões é coerente, existe sempre uma ligeira sobredensidade na transição.
Situação sanitária da exploração
Antecedentes
A exploração é indemne para Aujeszky e PRRS.
Em Junho de 2000 detectou-se um aumento da mortalidade na engorda passando de 3 para 5%, afectando maioritariamente os porcos que se encontravam no final desta fase. No matadouro detectou-se um aumento importante das rejeições (até 10% por lote) devido a pleuresias com abcessos. Decidiu~se enviar amostras pulmonares de animales que ainda se encontravam na exploração e de animais abatido para o laboratório. A análise bacteriológica acusou a presença de Actinobacillus pleuropneumoniae biovar 1 serovar 2 (B1S2). Após esta descoberta decidiu-se vacinar os animais com uma autovacina seguindo o seguinte protocolo vacinal:
- Leitões: 2 injecções às 6 e 10 semanas de vida.
- Primíparas: 2 injecções às 6 e 10 semanas de vida e 1 de rappel à entrada na quarentena.
- Porcas: 2 injecciones às 6 e 3 semanas antes do parto e em ciclos posteriores às 3 semanas antes do parto.
Ao fim de vários meses observou-se uma reducção da mortalidade e das rejeições. Contudo, no matadouro continuaram-se a observar lesões de pleuresia (até 30% dos pulmões).
Profilaxia e tratamento
| Profilaxia | |
| Porcas |
Mal Rubro: primíparas 2 vezes + rappel na maternidade (15 dias depois do parto) Parvovirus: primíparas 2 vezes + rappel na maternidade |
| Leitões | Micoplasma: 2 injecções aos 5 e 27 dias de vida |
| Tratamento | |
| Amoxicilina (20 mg/kg) no primeiro dia de vida | |
| Alimento de primeira idade com suplemento de calistenia (120 ppm) | |
Visita à exploração
Durante o Verão de 2002, o produtor avisa o veterinário após observar presença de animais fracos e tosse no pavilhão de transição em animais entre 5 a 6 semanas de vida, perdas de 6 a 8% devido a mortalidade e sacrificio de leitões com atrasos de crescimento e aumento do número de rejeições por pleuresia no matadouro.
Medidas cautelares
O veterinário decide tomar as seguintes medidas cautelares: tratar os leitões no momento do desmame cmn cefquinoma (2 mg/kg) por via parenteral e um suplemento de 400 ppm de amoxicilina na dieta de primeira idade.
Segunda visita à exploração
Na semana seguinte voltou-se a visitar a exploração e visitaram-se todos os pavilhões:
| Quarentena |
|
Cerca de 20% das primíparas apresentavam tosse. Ausência de imunização digestiva ou respiratória. Observou-se um desenvolvimento normal dos animais e sem problemas na entrada em cio. |
| Varrascos - gestação |
|
Sem problemas de entrada em cio. Fertilidade: 85%. Ausência de tosse. |
| Maternidade |
|
Resultados reprodutivos correctos. Bom comportamento maternal das mães. Diarreia neonatal sobretudo nas ninhadas procedentes de primeiros partos (nalgunas ninhadas a mortalidade é muito elevada). Nas 2 últimas bandas observa-se uma forte tosse aos 15 das de vida (15% em 2 minutos) assim como artrite (3% dos leitões). |
| Transição |
|
Presença de tosse nos animais de 6 semanas de vida (30% em 2 minutos) desde há 1 mês com atrasos no crescimentos e mortalidade entre 6 e 10%. Ausência de sinais digestivos. Cumprimento das normas técnicas e ambiente correcto. |
| Crescimento |
|
Ausência de sintomas digestivos ou respiratórios. Heterogeneidade nos animais devido aos problemas observados na transição. |
| Engorda |
|
Até 80 kg: Normal A partir de 80 kg: os porcos apresentam anorexia de curta duração (1 a 2 dias) e tosse forte (15% em 2 minutos). Ausência de mortalidade. Rejeições parciais no matadouro sobre um grande número de carcaças (7-8%). |
Exames complementares
Decidiu-se realizar um controle sobre um número significativo de carcaças no matadouro para ter uma ideia precisa da frequência das lesões observadas e origens das rejeições.
Por outro lado, praticaram-se alguns exames de laboratório para conhecer a origem das desordens e lesões observadas:
- Necropsias
- Análises bacteriológicas
- Análises serológicos para PRRS
- PCR para circovirus sobre lesões
Resultados dos exames
Resultados dos controles no matadouro
A maioria dos controles realizaram-se durante o mês de Setembro, em termos médios, entre 80 a 90% dos pulmões não apresentaram pneumonia enquanto que entre 30 a 50% apresentaram lesões de pleuresia. Entre 7 a 8% das cavidades torácicas foram rejeitadas.
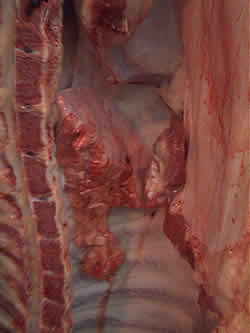 Pulmão colapsado (sem abcesso) |
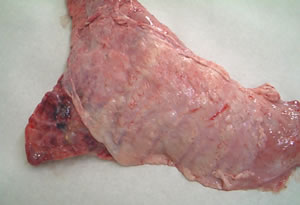 Pulmão com lesão de pleuresia com abcessos |
Exames laboratoriais
Leitões em lactação: realizou-se a necropsia em laboratório de leitão de 15 dias de vida. Observou-se presença de pneumonia e pleuresia leve. Isolou-se Bordetella bronchiseptica dos pulmões.
Leitões na transição: 3 leitões não tratados que tinham começado a apresentar sinais clínicos (tosse, emagrecimento) foram abatidos e enviados ao laboratório.
Necropsias:
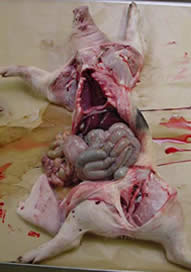 |
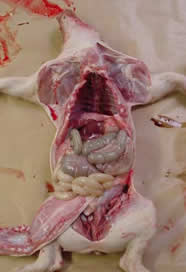 |
| Leitões de 40 dias necropsiados | |
- Exame circulatório e hemato-linfopoiético (coração, baço): Normal
-
Aparelho respiratório:
- Corte nasal: normal.
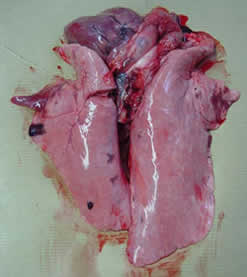
- Pulmões: lesões de pneumonia nos lóbulos (hepatização). Notas globais 10 a 22/28.
- Pleuresia num dos leitões.
- Aparelho locomotor: observa-se de forma geral uma ligeira inflamação de uma ou mais articulações.
- Aparelho digestivo: normal
 |
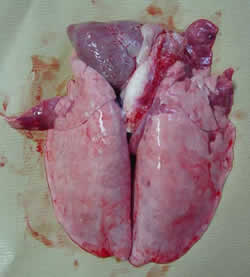 |
| Pulmões com presença de lesões de pneumonia a nível dos lóbulos apicais e cardíacos. Ausência de pleuresia. | |
 |
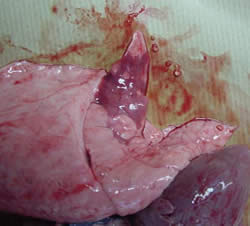 |
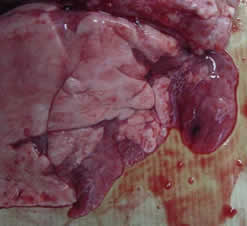
| Hepatização encarnada e atelectasia do tecido pulmonar | |
Bacteriologia:
- Pulmões: Isola-se Haemophilus parasuis em 2 de 3 leitões (nas lesões de pneumonia).
- Articulações: Não se evidenciou a presença de nenhum gérmen significativo nas lesões de artrite.
- Bacteriologia sobre pulmões recolhidos no matadouro: isolou-se; Actinobacillus pleuropneumoniae B1S2.
Análises serológicas para PRRS
- Realizaram-se serologias em 10 leitões de 25 kg e 10 porcos de engorda de 100 kg e todas as análises foram negativas.
PCR para circovirus sobre lesões
- PCR Circovirus tipo 2 sobre pulmões e gânglios: todas as análises foram negativas.
Diagnóstico
Devido à ausência de PCV2 nos tecidos lesionados a circovirose foi excluida das hipóteses sobre o diagnóstico, de forma que os sintomas de atraso no crescimento observados na transição provavelmente não se podem ligar com presença do sindrome do atraso de crescimento (PMWS).
O isolamento de Bordetella bronchiseptica de pulmões de um leitão lactante, de Haemophilus parasuis nas lesões de pneumonia de leitões na transição e de Actinobacillus pleuropneumoniae nas lesões de pleuresia dos pulmões recolhidos no matadouro fez suspeitar de uma infecção pulmonar multifactorial.
Medidas tomadas e Evolução 1. Alojamento das primíparas na quarentena:
- Contaminação digestiva: exposição a excrementos de porcas na maternidade de 2 a 3 vezes por semana durante toda a quarentena.
- Contaminação respiratória: contacto nariz com nariz com uma porca de refugo (em bom estado de saúde).
2. Instauração de uma nova autovacina:
Reprodutores:
- Actinobacillus pleuropneumoniae B1S2 (estirpe isolada em Outubro de 2002).
- Haemophilus parasuis (estirpe isolada em Novembro de 2002).
-
Bordetella bronchiseptica (estirpe isolada em Novembro de 2002).
==> 2 injecções (5 ml) nas porcas às 6 e 3 semanas antes do parto e em ciclos posteriores uma 3 semanas antes do parto.
==> 2 injecções (2 ml) nas primíparas às 7 e 11 semanas de vida e dose de rappel (2 ml) à entrada na quarentena.
Demais animais:
- Actinobacillus pleuropneumoniae B1S2 (estirpe isolada em Outubro de 2002).
-
Haemophilus parasuis (estirpe isolada em Novembro de 2002).
==> 2 injecções (2 ml) às 7 e 11 semanas de vida.
Observação: a vacinação atrasou-se uma semana com a finalidade de proteger os porcos durante o maior tempo possível.
3. Instauração de tratamentos antibióticos nos leitões à espera do efeito esperado da vacinação.
- Leitões lactantes: amoxicilina (20 mg/kg) durante o primeiro dia de vida via parenteral + Oxitetraciclina LO (30 mg/kg) no momento do desmame por via oral.
- Leitões na transição: suplementação da dieta de primeira idade com 400 ppm de amoxicilina.
- Crescimento: nenhuma intervenção.
- Engorda: marbofloxacina (2mg/kg) 3 vezes com um intervalo de 24 horas nos animais que tenham sintomas até aos 150-160 dias de vida.
4. Desinfecção do ambiente
- Com a finalidade de diminuir a pressão de infecção no ar nos pavilhões de transição, crescimento e engorda, uma vez por dia pulveriza-se um desinfectante.
Evolução do caso
Na actualidade a patologia ficou estabilizada graças à prevenção mediante antibióticos. Deverá realizar-se um acompanhamento dos resultados durante os meses seguintes com a finalidade de poder avaliar o efeito da auto-vacinação e da contaminação das primíparas.
Comentários
O caso aparece numa exploração de ciclo fechado e deve-se a uma infecção pulmonar polimicrobiana (Actinobacillus pleuropneumoniae, Haemophilus parasuis y Bordetella bronchiseptica). Este caso da lugar à posteriori a vários comentários:
O esquema seguinte resume o papel dos diferentes agentes patogénicos existentes nesta exploração:
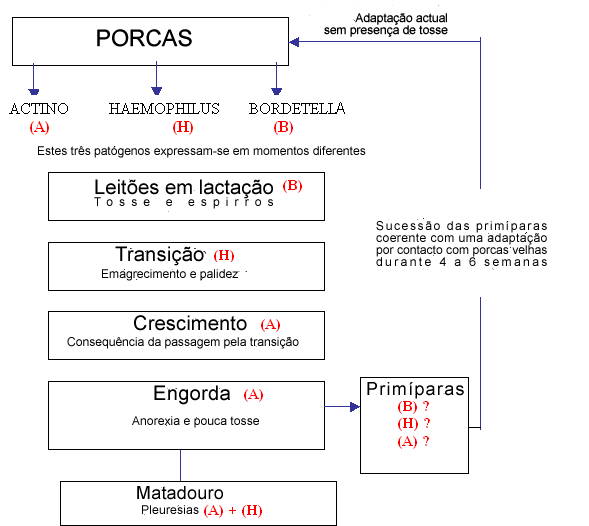
As primíparas, ainda que procedam da messma exploração (auto-substituição), possuem um microbismo próprio e portanto um status imunitário muito diferente ao das porcas que se encontram em producção. É por isso que se torna necessário conseguir uma imunização ao nível digestivo e respiratório. Desta forma, as primíparas desenvolvem uma imunidade que poderão transmitir aos seus leitões após o parto. Mediante este tipo de medida espera-se oferecer uma melhor protecção aos leitões contra os gérmenes digestivos (responsáveis pela diarreia) e gérmenes respiratórios (responsáveis pela tosse na maternidade e na transição.
As primíparas são portadoras de Actinobacillus pleuropneumoniae B1S2 e a autorenovação é um obstáculo para o saneamento da exploração. Neste ponto devemos perguntar a nós mesmo sobre que medidas nos permitirão parar a circulação deste gérmen entre os reprodutores, ¿a autovacinação será suficiente?
A PCR para circovirose permitiu-nos confirmar a ausência de PMWS. Este método, ainda que controverso, pareceu ser uma ferramenta interessante no diagnóstico desta patologia.
Relativamente a Haemophilus parasuis, este mostrou ter uma virulência particular na transição nesta exploração indemne para PRRS e PMWS. Chegados a este ponto poderíamos perguntar pela existência de estirpes de Haemophilus parasuis hiperpatogénicas.Por otro lado, ¿que importância devemos conceder à presença de Bordetella neste caso?
