Perguntas frequentes sobre o vírus da PSA detetado em Barcelona
06-Mai-2026 (há 22 dias)
Como são classificados os vírus da PSA?
O vírus da peste suína africana (PSAv) foi classificado em vários genótipos com base na sequência do gene B646L, que codifica a proteína p72, um componente principal do vírus. Com base nesta sequência, foram descritos até 24 genótipos distintos, a circular no continente africano.
Fora de África, apenas foram relatados os seguintes:
- Genotipo I: a circular atualmente na Ásia e responsável pela pandemia originada nos anos 60s.
- Genotipo II: o maioritário na atual pandemia, iniciada na Georgia no ano 2007.
O laboratório de referência europeu propôs a classificação por grupos genéticos dentro do genótipo II com base nas diferenças nas sequências de seis regiões variáveis do genoma do vírus.
| CVR | IGR I73R/I329L | O174L |
| K145R | IGR MGF505 9R/10R | IGR I329L-I215L |
Com base nas diferenças encontradas nestas regiões, foram descritos um total de 28 grupos genéticos, sendo o grupo genético # 1 representado pela estirpe Georgia2007.
A nomenclatura proposta para a estirpe encontrada em Barcelona é SP25WB2611, abreviada como Sp25.
A estirpe encontrada em Barcelona (Sp25) é diferente das conhecidas até ao momento e, por esse motivo, foi classificada num novo grupo genético, o #29.
Alguns grupos genéticos foram isolados apenas de porcos domésticos, outros apenas de javalis e outros ainda de ambos os animais. Os grupos genéticos, como o #3 ou o #19, são encontrados em diferentes países, mas a maioria foi detetada apenas numa área geográfica específica. Da mesma forma, existem áreas onde circula mais do que um grupo genético, como na Federação Russa (#1, #2, #3, #4 e #7) ou na Roménia (#3, #7, #19, #21, #22 e #24).
O genoma da estirpe Sp25 apresenta uma grande deleção, de aproximadamente 10 kb, na extremidade esquerda do genoma e, além disso, um total de 27 SNPs (polimorfismos de nucleótidos únicos) em comparação com a estirpe Georgia 2007.
Como é que as sequências disponíveis no Genebank, com as quais as novas linhagens são comparadas, estão distribuídas no tempo e no espaço?
Embora muitas estirpes de PSAv tenham sido isoladas na Europa desde 2007, o número de sequências obtidas é comparativamente muito baixo.
O conhecimento sobre a distribuição geográfica dos grupos genéticos depende do número de amostras sequenciadas e publicadas em cada país. Em muitos países afectados pela peste suína africana (PSA), as amostras não são sequenciadas e/ou os resultados não são publicados.
As análises de sequência da estirpe Sp25, realizadas no IRB e BSC em Barcelona, mostram a sua proximidade filogenética com estirpes isoladas de surtos em países europeus após a introdução do vírus Georgia no continente em 2007 (Figura 1). A estirpe Sp25 parece pertencer a uma linhagem que divergiu muito cedo e, por isso, é muito diferente daquelas que causaram os surtos mais recentes na Europa central e ocidental. Como mostra a árvore filogenética, esta sequência está mais relacionada com vírus detetados na Rússia em 2019 do que com estirpes isoladas na Europa central e ocidental, mas continua a ser muito diferente de qualquer estirpe para a qual tenha sido obtido o genoma completo, incluindo as isoladas da Rússia, das quais difere na deleção mencionada e em mais de 20 SNPs.

O vírus da PSA é considerado um vírus de ADN muito grande e muito estável. Quantas alterações deve apresentar um isolado de PSA para ser considerado uma estirpe distinta?
No âmbito do PSAv na Europa, o Laboratório de Referência Europeu considera um isolado viral como uma estirpe distinta quando este é classificado como um novo grupo genético.
O número de SNPs que foram detetados permite observar a divergência temporal de uma estirpe em relação à estirpe "original" Georgia 2007. O PSAv é um vírus de ADN de cadeia dupla e, portanto, um vírus muito estável. Dada a baixa taxa de mutação do vírus, os vários SNPs presentes em Sp25 devem ter-se acumulado ao longo de um período prolongado desde a sua divergência da Georgia 2007. De acordo com as estimativas mais recentes, este período poderá ser de cerca de 10 a 15 anos de divergência evolutiva (estimativa feita pelo Dr. Toni Gabaldón, IRB).
Se o vírus é tão estável, poderá a deleção de 10.000 pares de bases observada no foco de Barcelona ocorrer naturalmente?
A própria dinâmica evolutiva natural do vírus gera este tipo de deleções genéticas. Dentro do genótipo II, já tinham sido descritas deleções na mesma região com diferentes extensões e envolvimento de genes, tanto em África (Ambagala et al., 2023) como na Europa (Zani et al., 2018; Torresi et al., 2025).
Esta deleção é utilizada em algumas vacinas candidatas. Isso significa que não pode ocorrer naturalmente?
Estes tipos de deleções no genoma do PSAv ocorrem naturalmente e também podem ser gerados em laboratório para criar alguns candidatos a vacinas. De salientar que, atualmente, durante o protocolo de desenvolvimento laboratorial de um candidato a vacina, um marcador exógeno é incluído no genoma viral na maioria dos casos (por razões técnicas) para o diferenciar da estirpe original. Portanto, os candidatos a vacina são facilmente identificáveis através de sequenciação. A estirpe Sp25 não possui qualquer tipo de marcador exógeno. Além disso, a maioria dos candidatos a vacina é gerada a partir de um pequeno grupo de estirpes laboratoriais muito semelhantes entre si e ao primeiro isolado do surto actual, Georgia2007.
A recombinação é comum entre as diferentes estirpes de PSA?
Para que estas recombinações ocorram, uma célula hospedeira tem de ser infetada simultaneamente por duas estirpes diferentes. Este fenómeno não é tão comum como nos vírus de RNA com genomas fragmentados (como o vírus da gripe), mas pode ocorrer com o PSAv. Foram reportadas recombinações entre os genótipos I e II na China (Zhao et al., 2023), e o mesmo vírus recombinante espalhou-se para outros países (Rússia e Vietname). Logicamente, quanto maior for o número de estirpes diferentes a circular na mesma área, maior será a probabilidade de tais recombinações. O padrão de mutação detectado na estirpe Collserola está distribuído por todo o genoma, e não numa região limitada, tornando improvável uma origem por recombinação.
Muito se fala sobre a estirpe detetada em Barcelona não ser muito virulenta. Será mesmo esse o caso?
A deleção identificada na estirpe Sp25 pode estar associada a uma menor virulência, como demonstrado noutras estirpes com deleções que afetam esta região. No entanto, existem exemplos de estirpes altamente virulentas com deleções semelhantes, pelo que esta conclusão não é definitiva. A virulência da estirpe Sp25 só pode ser avaliada através de infeção experimental em suínos ou javalis em condições controladas.
A única certeza que temos neste momento é que se trata de uma estirpe letal em javalis e que o padrão da doença observado é comparável ao descrito noutros focos europeus causados por estirpes classificadas como altamente virulentas.
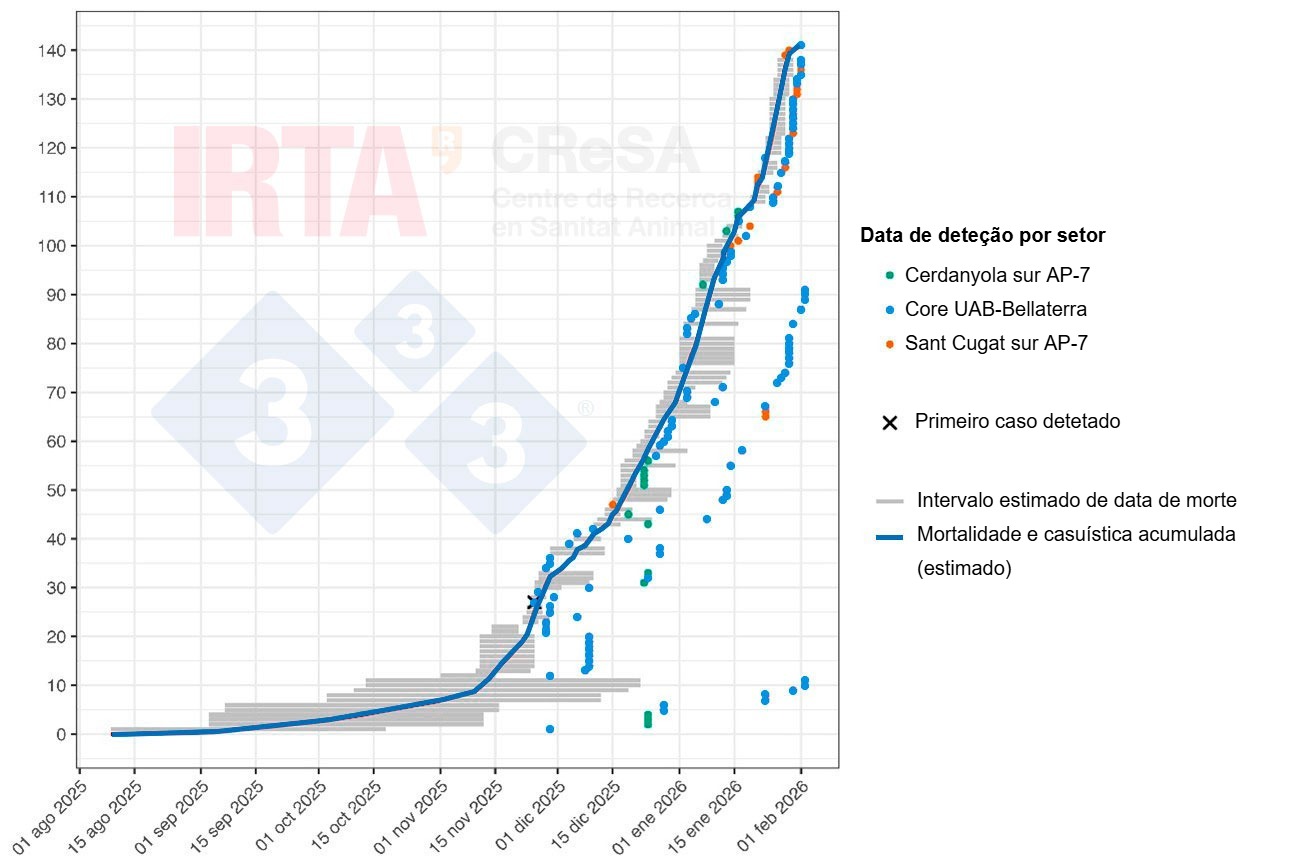
A Figura 2 mostra uma reconstituição cronológica dos casos de peste suína africana (PSA) em javalis no foc atual, considerando que a data em que a carcaça é encontrada não coincide, geralmente, com a data da morte. Para cada caso, é apresentado um período plausível para a morte do javali, estimado com base no estado de conservação da carcaça. Assim, embora a data exata das primeiras mortes não possa ser determinada com precisão, os períodos estimados para as primeiras carcaças indicam que a mortalidade associada ao surto começou meses antes da deteção do primeiro caso, provavelmente por volta de setembro. Portanto, a PSA circulou sem ser detetada durante um período inicial, provavelmente a níveis baixos, mas constantes, até ser detetada. A fase inicial, de progressão lenta, do surto corresponde à introdução e ao estabelecimento da PSA na população de javalis, seguida por uma fase epidémica na qual se observa uma mudança na inclinação da curva. De salientar que esta evolução não difere muito das observadas recentemente na Europa.