Etiología y epidemiología del virus de la Influenza porcina
Carlos Casanovas, Salvador Oliver, Sonia Cárceles, Laura Garza y David Espigares. Servicio Técnico Porcino CEVA Salud Animal
Introducción
El virus de la Influenza Porcina (SIV, de Swine Influenza Virus) es un agente patógeno primario de distribución mundial que afecta a una elevada proporción de granjas con mayor o menor gravedad. Juega un papel importante dentro del Complejo respiratorio porcino (CRP) y puede afectar a todas las fases productivas.
Es un virus con una elevada capacidad cambiante. Desde 1979 hasta hoy en día, tan solo en Europa, se han adaptado 4 linajes de hemaglutinina distintas a la especie porcina, lo que representa aproximadamente la introducción de un virus significativamente distinto cada década, lo que obliga a ir actualizando las vacunas de forma periódica.
En este artículo veremos el origen de esta variabilidad, debida fundamentalmente a la capacidad de la especie porcina de adaptar virus de origen humano y en menor medida aviares y al fenómeno de la reordenación genética de los virus Influenza.
Etiología de SIV
SIV es un virus ARN segmentado en 8 partes que codifican 11 proteínas:
- Dos externas: la Hemaglutinina (HA) y la Neuraminidasa (NA). La HA es la responsable de la unión del virus a la célula y la NA de su salida, por lo que ambas, pero especialmente la HA, son las principales responsables de la infección y la respuesta inmunitaria. La HA y la NA también sirven para clasificar a los virus en distintos subtipos: H1N1, H1N2 y H3N2, que son los más prevalentes en el caso del porcino.
- Nueve internas. Las proteínas internas juegan un papel importante en los distintos grados de virulencia de SIV.
Mecanismos de evolución
SIV es un virus cambiante debido a dos motivos, la deriva antigénica (antigenic drift) y la capacidad de reordenación (genetic shift).
Deriva antigénica
Ocurre por errores en la transcripción del virus, al igual que sucede con el virus del síndrome respiratorio y reproductivo porcino (PRRS, por sus siglas en inglés), pero con una tasa de mutación mucho más baja. Estos cambios aleatorios en la secuencia de nucleótidos pueden llevar (o no) a modificaciones en la estructura del virus que afecten a su virulencia o a su capacidad de escapar a la respuesta inmunitaria existente. Cuando esto ocurre, la cepa mutante tendrá más ventajas y tenderá a establecerse en la población, desplazando a la anterior.
La deriva es menor en la especie porcina que, por ejemplo, en la especie humana. Esto sucede porque en las granjas siempre suele haber animales candidatos a infectarse (reemplazos que entran negativos a SIV o a los subtipos que circulan en la granja, nacimiento constante de lechones, mezcla de animales con distinto estatus inmunitario al destete…), lo que permite que las cepas de SIV no se vean tan forzadas a evolucionar para persistir en la población.
Reordenación
Sucede cuando dos cepas distintas de SIV infectan al mismo tiempo una célula e intercambian segmentos genéticos entre sí (figura 1). Al contrario de la deriva antigénica, la reordenación sucede con mayor frecuencia en la especie porcina que en la humana debido al sistema de producción, con elevado número y densidad de animales susceptibles alojados en un mismo espacio, que aumenta mucho las posibilidades de coinfecciones con cepas de subtipos distintos. A esto se le suma que es habitual que las granjas estén infectadas por más de un subtipo al mismo tiempo.
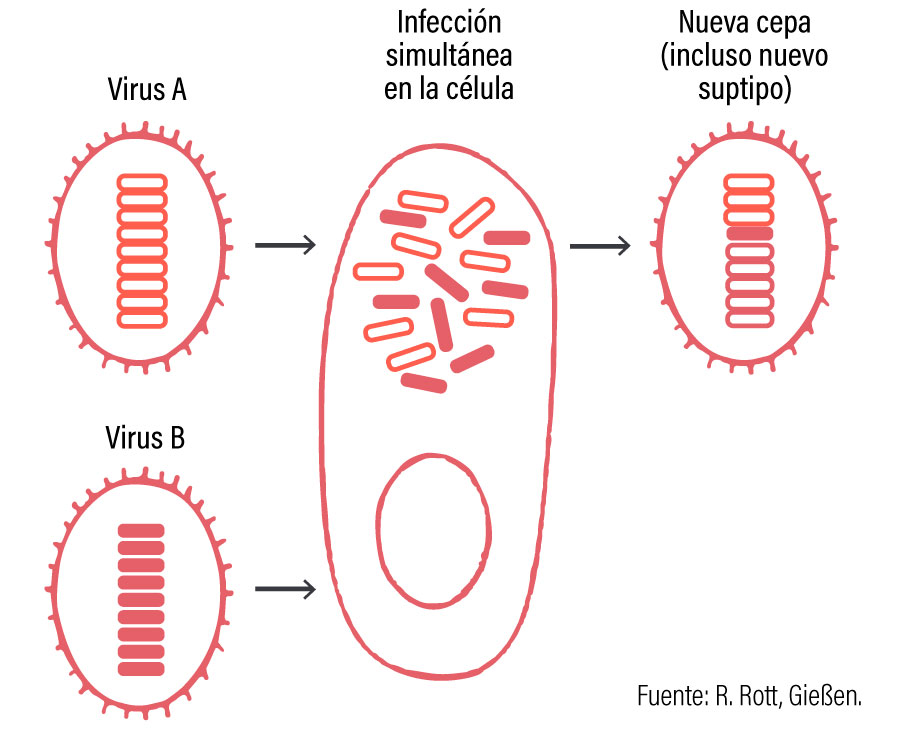
Las reordenaciones pueden suceder a nivel de los genes que codifican para las proteínas externas (HA y NA) y, como veremos a continuación, esto ha generado la diversidad de subtipos que circulan hoy en día. También veremos que estas reordenaciones pueden suceder a nivel de los genes que codifican para proteínas internas, como es el caso del linaje H1N1 pandémico.
Evolución de los distintos subtipos y linajes de SIV en Europa
El H1N1 que circula hoy en día en Europa y Asia es de origen enteramente aviar (los ocho segmentos). Esto sucede porque el cerdo es capaz de infectarse tanto de la especie humana como de las aves y ocasionalmente, como sucedió en este caso, acabar adaptando un virus totalmente nuevo a la cabaña porcina. Este H1N1 se denomina H1avN1 debido a su procedencia aviar y empezó a circular en 1979, cuando desplazó al H1N1 de origen humano que circulaba hasta entonces (figura 2).

El subtipo H3N2 es fruto de una reordenación entre un H1avN1 y un H3N2 de origen humano. En este caso, los seis segmentos que codifican para proteínas internas se mantuvieron (de origen aviar) y se adaptaron las HA y NA humanas, Este H3N2se denomina H3huN2 y se empezó a detectar en 1984.
El subtipo H1N2 se generó en 1994 como consecuencia de la reordenación entre un H3huN2 y un H1N1 de origen humano; en este caso se incorporó la HA exclusivamente. El subtipo resultante se denomina H1huN2 y es importante resaltar que no tiene una buena protección cruzada con H1avN1 porque, a pesar de que ambas HA de tipo H1 se parecen poco, provienen de especies distintas. Así pues, la introducción de este nuevo subtipo implicó la necesidad de actualizar las vacunas presentes hasta ese momento para obtener una protección global frente a SIV.
El linaje H1N1 pandémico (panH1N1) circula en la especie humana y porcina a nivel mundial desde el año 2009. Este virus se generó en la especie porcina tras múltiples reordenaciones entre virus de origen porcino, aviar y humano; el resultado fue un coctel donde tenemos presencia de: HA de origen porcino (pero procedente de América del Norte, donde no se llegó a introducir la H1av), NA procedente del H3huN2 euroasiático y genes internos aviares, porcinos y humanos, la mayoría de ellos norteamericanos. Este virus fue capaz de saltar la barrera interespecie con facilidad y de afectar a la población humana, que ha sido la responsable de su diseminación a nivel mundial y de provocar una pandemia (epidemia a nivel mundial). Ahora el virus ya está plenamente establecido en la cabaña porcina mundial fruto de su facilidad de transmisión entre ambas especies. De nuevo, la circulación de este nuevo linaje de H1N1, que es distinto al H1avN1 que circulaba hasta el momento, obliga a adaptar las vacunas existentes hasta el momento si se desea obtener una protección total.
La segregación entre continentes hace que SIV haya evolucionado de forma distinta en las áreas de mayor densidad porcina: Europa, América y Asia. Esto añade variabilidad a nivel mundial y hace que, como sucede en el caso del H1panN1, ciertos segmentos de genes procedentes de otras zonas del mundo lleguen, de forma puntual, a otras zonas muy distantes.
Reordenaciones entre subtipos y linajes que circulan en Europa
El tema de los subtipos y las reordenaciones es algo más complicado porque hay que añadir que los tres subtipos circulantes (H1avN1, H1huN2, H3huN2) son capaces de reordenarse entre sí y, desde el 2009, también con el linaje H1panN1
La figura 3 solo refleja reordenaciones entre distintas HA y NA ya que incluir todas las posibilidades, teniendo en cuenta los seis genes que codifican frente a proteínas internas, aumentaría enormemente las combinaciones. Además, tal como ya hemos dicho, la HA y NA son las más importantes desde el punto de vista inmunológico y son las que detectamos de forma habitual porque se pueden identificar mediante PCR.
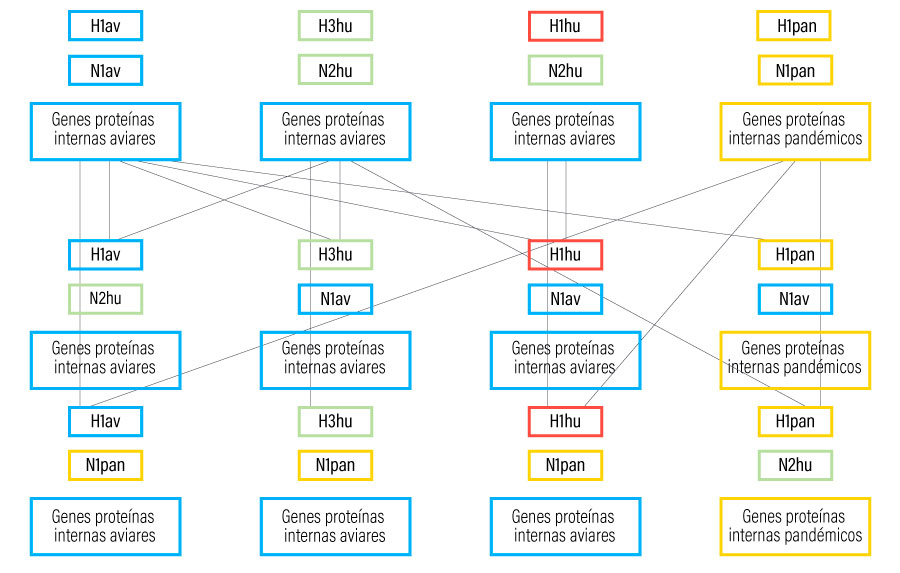
Hasta la presencia del H1panN1, los genes internos de los distintos subtipos de SIV europeos establecidos en la población porcina eran siempre aviares, procedentes del H1avN1. Sin embargo, desde la aparición de H1panN1 en 2009, sus HA y NA así como sus genes internos se reordenan con los subtipos que ya circulaban anteriormente (H1avN1, H1huN2 y H3huN2) y generan nuevas combinaciones de SIV que, potencialmente, podrían tener algunas ventajas biológicas que les permitiera ser más agresivas. La identificación de estos genes que codifican para proteínas internas ya no se puede hacer por PCR, requiere de secuenciación
Vemos que hay muchas combinaciones potenciales distintas y que a priori esta variabilidad parecería imposible de cubrir mediante una sola vacuna. Sin embargo, al final se trata de combinaciones entre “17 cartas de la misma baraja”:
- Ocho segmentos genéticos del H1avN1.
- Dos del H3huN2 (porque seis son iguales al H1avN1).
- Uno del H1huN2 (porque siete son iguales al H3huN2).
- Seis segmentos del H1panN1 (porque dos son iguales al H1avN1).
Podemos hacer muchas combinaciones distintas de ocho segmentos genéticos con los 17 que tenemos pero, al final, si tenemos todas las cartas de la baraja, una vacuna que ofrezca protección frente a todos los subtipos y linajes circulantes, cubrimos todas sus combinaciones.
Conclusión
SIV evoluciona de forma constante debido a la deriva genética que hace que el virus vaya cambiando poco a poco, en menor medida que en la especie humana, pero de forma continua. Su capacidad de reordenación y el hecho de que el porcino se pueda infectar a partir de virus de origen humano, y en menor medida de origen aviar, hace que puntualmente se den grandes cambios importantes a nivel de SIV. Estos cambios pueden ocurrir a nivel de hemaglutinina y neuroaminidasa, lo cual produce que se adapten nuevos subtipos al cerdo, pero también a nivel de genes que codifican para proteínas internas. En Europa, tales cambios se han descrito cuatro veces en aproximadamente los últimos 40 años. Cuando esto sucede, las vacunas comerciales de SIV se deben adaptar para continuar ofreciendo una protección lo más eficaz posible.
Artículo publicado en Suis nº 166 - Abril 2020
Bienvenido a 3tres3
Conecta, comparte y relaciónate con la mayor comunidad de profesionales del sector porcino.
¡Ya somos 137883 Usuarios!
Regístrate¿Ya eres miembro?