蓝耳病(PRRS)的分子诊断中,当测序覆盖率仅达4%时是不够的。
05-11月-2025 (之前 6 月 27 天)
猪蓝耳病病毒(PRRSV)与非洲猪瘟病毒一道,是影响全球养猪业经济效益最重要的病原之一。近来出现的PRRSV强毒株如亚洲的高致病性PRRSV(HP-PRRSV)、欧洲的Rosalia毒株和北美的LIC.5毒株,引发了关于进一步改善PRRSV诊断和控制的必要性的讨论。
利用反转录聚合酶链式反应(RT-PCT)检测PRRSV遗传物质被广泛用于群体中病毒的筛查。
比RNA检测更进一步的是PRRSV基因测序,通常利用Sanger测序技术来实现。总体来说,病毒基因中常用于PRRSV测序的是ORF5片段,但也有些实验室使用ORF7片段。
PRRSV基因组中,ORF5片段占约4%,而ORF7占约2.4%。因此,二者均不能完全覆盖全基因组的遗传信息。
近年来,人们越来越感兴趣的是,使用下一代测序(NGS)来恢复PRRSV全基因组,为农场或生产体系中PRRSV的流行病学调查提供支持(图1)。
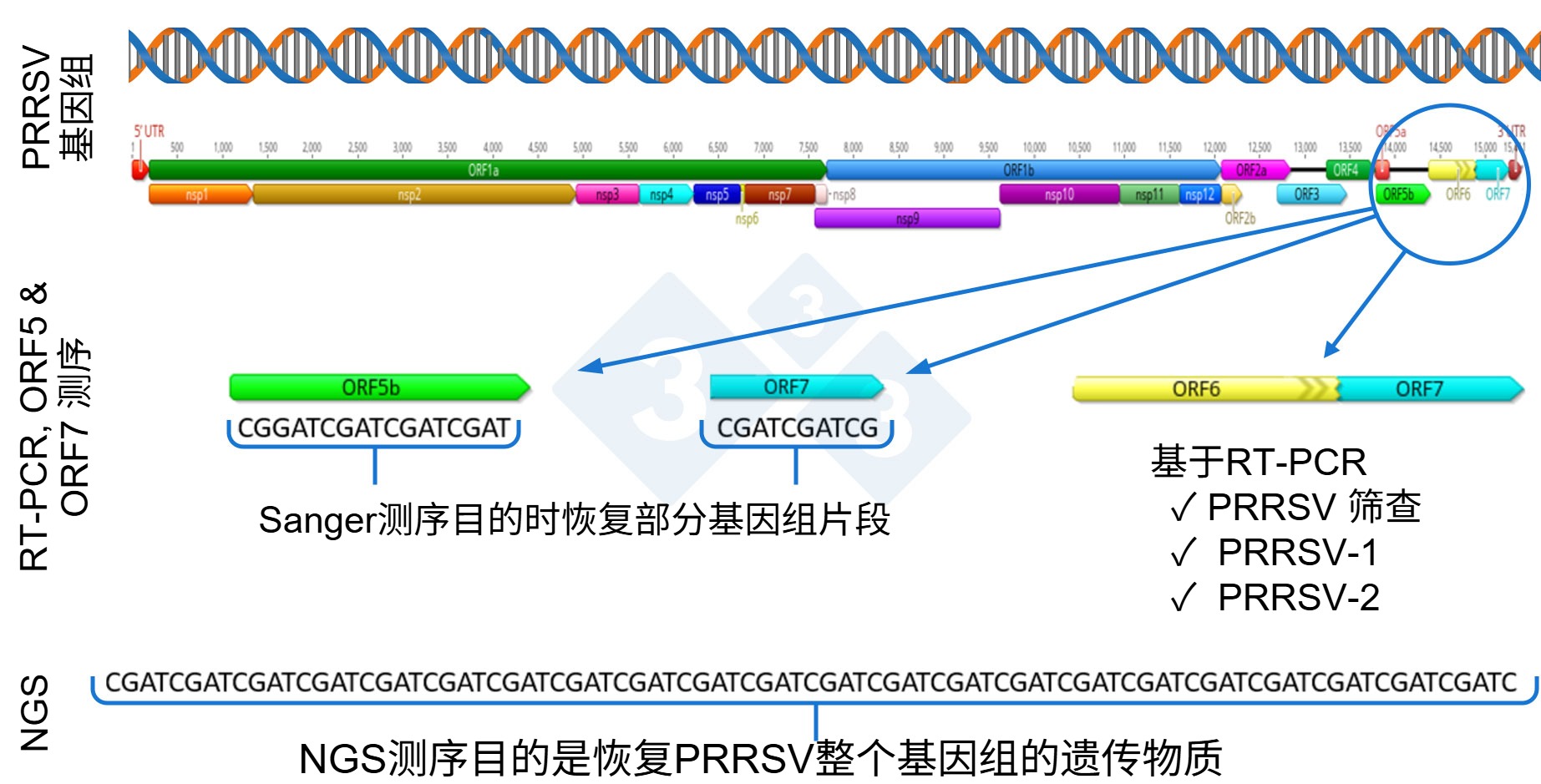
一般来说,在复制过程中PRRSV会经历基因改变和变异,这可能潜在地导致新的病毒变异株的出现。PRRSV是已知具有高突变率的病毒之一,约每年0.5%-1%,并在不同基因组区域、病毒类型和遗传谱系中不均匀分布,导致持续的遗传进化。值得注意的是,基因变异和病毒进化可能发生在所有的基因,仅仅测序基因组的一个片段,如ORF5或ORF7,很可能会错过测序区域外的变化(图1)。
这种情况下,NGS就成为十分有用的工具,能够恢复PRRSV的全部基因组以支持流行病学调查。
兽医和生产者如何利用NGS
想要最大程度利用NGS,需要考虑以下因素:
- 兽医和实验室诊断技术人员的早期参与对于理顺诊断问题、预期和检测方法非常重要。
- 农场或生产体系中是否存在用于对照的PRRSV参考毒株全基因组序列?
- 如果没有,则使用NGS方法检测PRRSV RT-PCR阳性且Ct值较低的样品,如Ct值小于24的理想条件下,从而恢复整个基因组以作为农场参考毒株。Ct值和样品中病毒的基因拷贝数呈负相关,Ct值越低则预期的病毒载量和NGS潜在的成功率越高。
- 参考毒株允许对前瞻性恢复的基因组进行后续对比,以理解PRRSV在农场、跨场流动和生产体系中的遗传进化。
- 做NGS测序的目的是什么?
- 如果目的是在全基因组水平上检测病毒的进化:则靶标在肺脏和血清上,因为这些样品更有可能用于恢复病毒全基因组。
- 如果目标是在农场或动物群体中了解病毒的多样性,则使用群体样品类型,如处理液、口腔液样品或单个样品的混样,比如血清混样更容易恢复样品中存在的多种病毒。
- 动物群体种混合感染两种及以上PRRSV病毒毒株已是事实(图2a),如果这两种病毒很类似,NGS测序则可能无法恢复全基因组。
- 如果样品种存在多种病毒,NGS可能从不同的病毒中恢复基因组片段,即“contigs”,当与农场中的参考毒株进行对比时,该基因组片段能帮助识别样品中是否存在多种病毒(图2b)。
- 最后,确定有人能帮助进行基因分析和比对,并协调周转时间,因为NGS测序是一个耗时的过程,一般需要一周以上才能完成。

从NGS结果中我们能得到哪些流行病学信息?
产生的NGS结果能帮助解决以下问题:
- 病毒进化是否通过同一基因组位点上的随机核苷酸替代实现的?对比两个时间点,病毒改变了多少?这些改变发生在哪个基因组,比如ORF区域?
- 病毒进化是否通过基因组中的插入或缺失实现的?
- 在农场、畜群或人员流动中是否新引入了无关的病毒?
- 尽管不太会发生但仍然有可能发生,新病毒是否在RT-PCR或Sanger引物/探针测序的基因组区域发生了变化,导致检测失败?
- 病毒是否进行了重组,如从从两个或多个亲本病毒中获得一些基因组片段?
重组时PRRSV进化的自然过程,当两种PRRSV在同一个细胞内复制就会产生第三种病毒。病毒重组的话题将在pig333.com网站上2025年6月9日发表的文章“The implications of the PRRSV recombination dilemma”中进一步讨论。
