Descripción de la granja
Se trata de una granja de multiplicación de 250 cerdas en la región polaca de Gran Polonia, en la que todas las cerdas que servirán para reposición se mantienen hasta que alcanzan los 100 kg. Los machos y las cerditas descartadas se venden a un engorde tras el destete. Se utiliza inseminación artificial. Se trabaja con grupos tecnológicos de 10 cerdas gestantes y los lechones se destetan a los 28 días, manteniendo el sistema "todo dentro-todo fuera". Aproximadamente se destetan 6.200 lechones cada año.

En el momento de la aparición del caso las condiciones ambientales de la granja eran buenas y el estado sanitario se consideraba muy alto: era negativa a Brachyspira hyodysenteriae, Salmonella spp. y Pasteurella multocida toxigénica, PRRSV, Actinobacillus pleuropneumoniae, Mycoplasma hyopneumoniae, Leptospira spp. y sólo positiva a Bordetella bronchiseptica y Lawsonia intracellularis. Tampoco se habían descrito casos de PMWS. La rutina profiláctica en las reproductoras incluía vacunación frente a colibacilosis (en nulíparas a las 8 y 3 semanas antes del parto y en cerdas a las 3 semanas) y frente a erisipelas y parvovirosis (nulíparas a los 5,5 y 6,5 meses de edad y en cerdas a las 3 semanas antes del parto). No se había vacunado frente a PCV2.
Aparición del caso
Durante la primera visita se observó muerte súbita de animales, también se observaron animales con un profuso edema facial en orejas y región pectoral (fig. 1), así como un aumento de la temperatura corporal hasta los 41,5 ºC. En algunos animales también se apreciaron síntomas neurológicos (opistótono, posición lateral, movimientos de remo en las patas). Inicialmente los síntomas se observaron en un grupo de nulíparas de 70-100 kg de peso. La morbilidad aumentó hasta más del 15 % y la mortalidad ascendió hasta más del 6 %. Durante el mes siguiente se observaron síntomas similares, pero con una intensidad ligeramente menor, y que afectaron a animales más jóvenes – transición y nulíparas hasta 70 kg. En las siguientes semanas se observaron síntomas parecidos (excepto los neurológicos) en cerdas destetadas y en la maternidad y lactación.
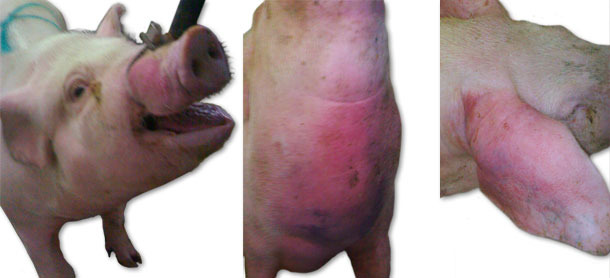
Fig. 1. Síntomas de edema.
Necropsia y tests laboratoriales
Se enviaron cuatro animales enfermos al laboratorio. Mostraban síntomas clínicos como un gran edema con fóvea en las partes más bajas, acumulación subcutánea de fluido en el área del esternón en dos lechones destetados (fig. 3) y temperatura de 41,0 a 41,3 ºC. La necropsia mostró una infiltración subcutánea gelatinosa, especialmente en las zonas más bajas (fig. 2, 3), pericarditis serofibrinosa (fig. 4) y pleuritis.
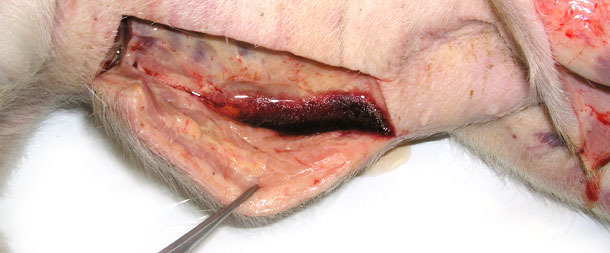
Fig. 2. Hinchazón del tejido subcutáneo, emerge una gran cantidad de fluido tras una incisión de la piel en la zona baja del cuerpo.
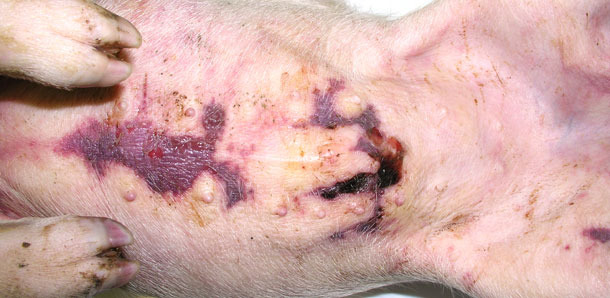
Fig. 3. Acumulación de fluido bajo la piel en el área esternal.
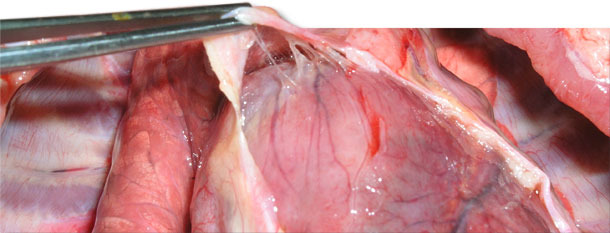

Fig. 4. Fibrina delicada y frágil entre el epicardio y el saco pericárdico.
Tras la valoración patológica, se realizó el examen bacteriológico. Debido a que no había cojeras ni síntomas nerviosos en los animales examinados, no se tomaron muestras de las articulaciones ni del fluido cerebroespinal. El material analizado se recogió asépticamente y los hisopos se tomaron al poco tiempo de abrir las cavidades corporales.
Las muestras se sembraron en agar de sangre de caballo con siembra de Staphylococcus epidermidis y en agar McConkey. La identificación se realizó con tests bioquímicos (Vitec) o mediante PCR.
Resultados laboratoriales
Los estudios bacteriológicos sólo mostraron crecimiento de Haemophilus parasuis (H. parasuis). Las colonias eran muy pequeñas (como pinchazos de alfiler), no hemolíticas, con satelitismo (aumento de las colonias) alrededor de la estría de Staphylococcus epidermidis (fuente de NAD).
Los hisopos tomados de los cambios patológicos (lechones destetados) se analizaron mediante PCR. Los resultados se muestran en la tabla 1.
Tabla I. Diagnóstico laboratorial de Haemophilus parasuis a partir de superficies serosas y suero.
| tejido | lechón 1 | lechón 2 | lechón 3 | lechón 4 |
| Aislado + PCR / PCR tejido | ||||
| pleura | +/+ | +/+ | +/+ | +/+ |
| pericardio | +/+ | +/+ | +/+ | +/+ |
| peritoneo | -/- | +/+ | -/- | -/- |
| suero | +/+ | -/- | -/- | -/+ |
Se confirmó la presencia de H. parasuis en las lesiones típicas de Glässer. También se identificó la bacteria, o su ADN (PCR), en suero, lo que demostró que dos de los cuatro lechones analizados presentaban bacteriemia.
Tras la detección de H. parasuis en los cuatro lechones necropsiados se tomaron 20 hisopos nasales de destetados, nulíparas y cerdas para comparar las cepas de los animales enfermos con la de los sanos (portadores). Se realizó un aislado e identificación de los microorganismos de los hisopos (identificación bioquímica y confirmación final de la cepa mediante PCR).
Se analizaron diez aislados de H. parasuis – cuatro de los animales necropsiados y seis de los sanos – mediante caracterización molecular por ERIC PCR (fig. 5). Todos los aislados que se obtuvieron de los animales enfermos tenían el mismo perfil ERIC PCR. Curiosamente, se encontraron cepas idénticas en las muestras nasales de dos de los seis animales sanos. Los cuatro restantes tenían distintas cepas de H. parasuis en la cavidad nasal, caracterizados por distintos perfiles ERIC PCR.
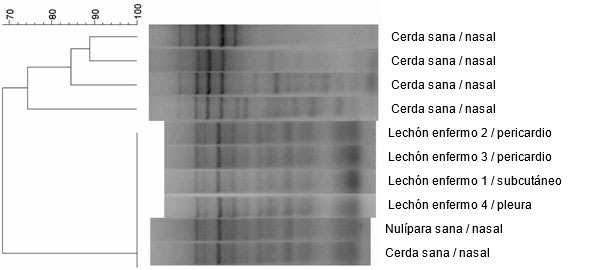
Fig. 5. Dendrograma que compara las cepas aisladas de H. parasuis mediante ERIC PCR.
Tratamiento
El tratamiento consistió en amoxicilina + ácido clavulánico i.m. en los animales con síntomas clínicos y en la implementación de un tratamiento metafiláctico con amoxicilina en agua de bebida (14 días, 20 mg/kg pv) en el resto de animales. Este tratamiento tuvo un resultado terapéutico permanente.
Conclusiones
En las explotaciones con elevado estado sanitario, la infección por H. parasuis a menudo se presenta de forma aguda, afectando a animales de cualquier grupo de edad. Los síntomas como fiebre, apatía, problemas respiratorios, dolor al presionar los músculos abdominales (defensa muscular), inflamación de las articulaciones y cojeras son característicos de esta forma de Glässer. También pueden observarse síntomas nerviosos y edema subcutáneo, como sucedió en este caso.
Los cambios patológicos descritos en este caso son característicos de una inflamación aguda serofibrinosa. Estos cambios no son patognomónicos, por lo que el diagnóstico debe basarse en el análisis laboratorial.
La específica localización del edema en las partes bajas del cuerpo, así como su carácter depresible (fóvea) hace pensar en un fallo cardíaco (edema cardíaco), concretamente en un fallo cardíaco congestivo con el consiguiente estancamiento de sangre en la circulación sistémica. Sin embargo, esta conclusión no concuerda con la presencia confirmada de H. parasuis en el tejido subcutáneo de este caso concreto. Esto podría sugerir hinchazón inflamatoria causada directamente por el agente bacteriano. Esto puede ser explicado por la bacteriemia: se detectó presencia de la bacteria en el tejido subcutáneo, procedente de vasos sanguíneos dañados.
La posibilidad de diferenciar entre cepas de H. parasuis circulantes en la granja puede ser importante ya que la epidemiología de H. parasuis es compleja y la infección que causa es un proceso dinámico. Por ello a menudo se utilizan varias técnicas de tipaje, lo que permite identificar entre distintas especies (ERIC PCR). En granjas con un buen estado sanitario predominan ciertas cepas que pueden causar la enfermedad. En el caso descrito se demostró que seis aislados tenían el mismo perfil ERIC PCR y pertenecían a una misma cepa patógena de H. parasuis. Su presencia también se confirmó en animales clínicamente sanos. Este hecho y el efecto terapéutico permanente del antibiótico (sin vacunación), podría indicar una inmunidad creciente en la granja contra nuevos casos clínicos por la misma cepa patógena.